14.婦人科領域におけるがん疼痛の治療法
・ 世界保健機関(WHO)が 1986 年( 1996 年改訂)提唱したがん疼痛治療ガイドライン1)は,あらゆる国でがんの痛みに対して実施されるべき基盤的なものとして啓発された.このガイドラインを遵守することで 8 割の患者でがんの痛みの軽減が可能であると報告されている2)が,実臨床ではこの基本中の基本だけで対処できない痛みが数多く存在する.
・ 本項では,オピオイドの使用に加えて,専門的ながん疼痛治療法について概説する.
(1)がん疼痛を目の前にしたら
・ 目の前に痛みを抱えている婦人科がんの患者に対し,「がんで痛いならオピオイド」と短絡的に考えてはいけない.
・ 表22 の順番に沿って対応を考える.
・ この順番に考えていかないと,余計な鎮痛薬を患者に投与することになる.

・以下,3 の鎮痛方法について述べる.
(2)鎮痛薬の全身投与
・ まずは,アセトアミノフェンと非ステロイド性抗炎症薬(NSAIDs:non-steroidal antiinflammatory drugs)で痛みが軽減できるか判断する.
・ アセトアミノフェン300㎎頓用という処方では鎮痛効果は期待できない.50㎏以上の体重の患者であれば800~1,000㎎× 4 回/ 日の定時投与にする.
・ NSAIDs は頓用で使用する.
【処方例】アセトアミノフェン1,000㎎× 4 回(定時)+ロキソプロフェン60㎎ 1 錠 頓用 1 日3 回まで
・ 痛みが軽減しない場合はオピオイドを検討する.
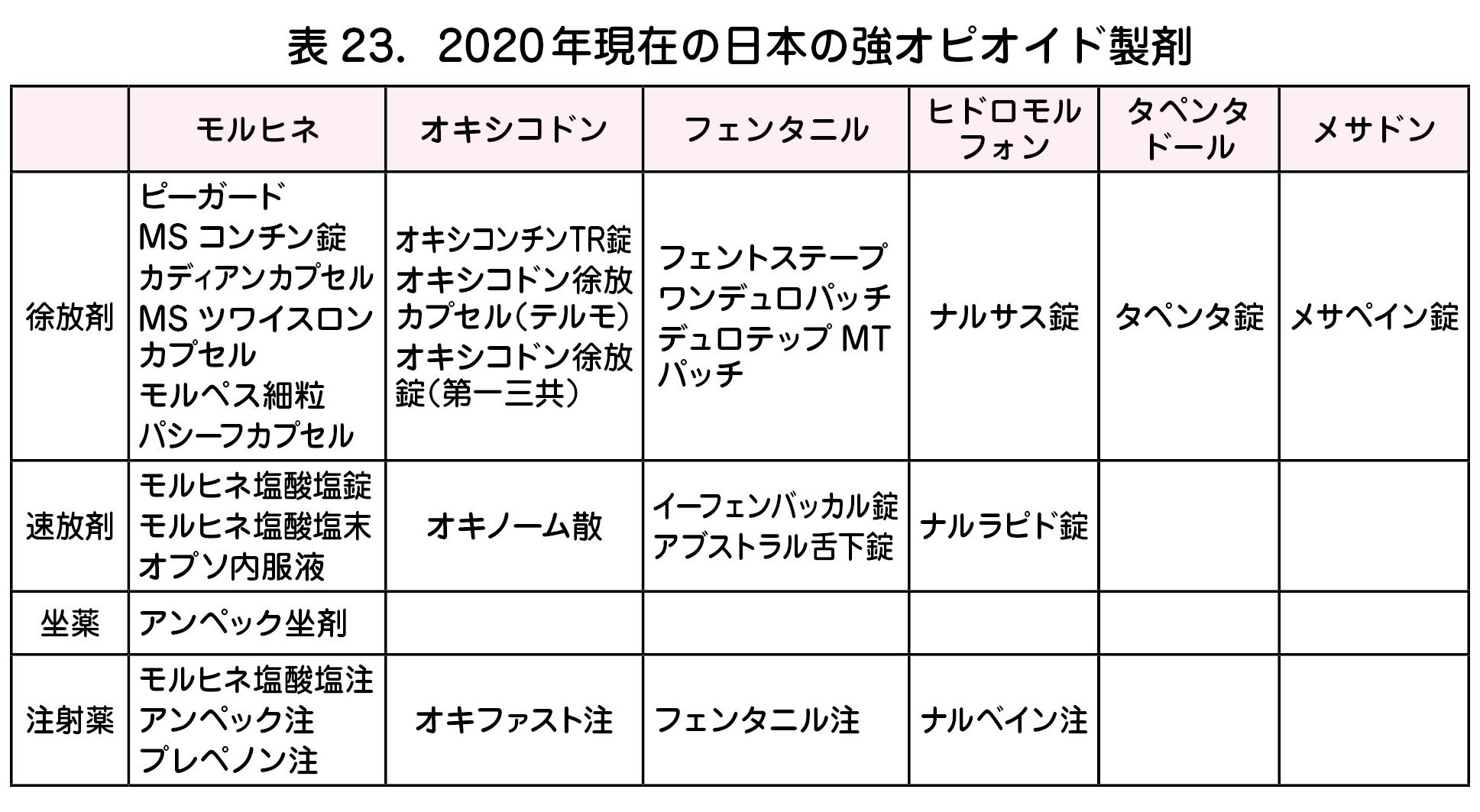
・ 2020 年現在,本邦で使用できるオピオイド製剤を表23 に示す.
ヒドロモルフォン,モルヒネ,オキシコドン,タペンタドールのいずれかで開始する.
フェンタニル,メサドンは,他のオピオイドからの切り替えでしか使用できない.
トラマドールは使用上限が低いため,進行性のがんの痛みには使用しないことが多い.
1 )ヒドロモルフォン:徐放製剤,速放製剤,注射薬
・ 日本では最近発売されたので新しい薬剤のように思われがちだが,WHO のガイドラインでも強オピオイド使用時の推奨として最初に名前が出てくるほど世界では一般化されているオピオイドである.
・ モルヒネから誘導された半合成麻薬であり,活性代謝産物が少ないため腎機能障害がある患者でも使用しやすい薬剤である.モルヒネに代わる製剤として使用が広がっている.
2 )モルヒネ:徐放製剤,速放製剤,坐剤,注射薬
・ 昔から日本でがん疼痛に使用されてきたオピオイドであり,すべてのオピオイドの基準薬である.
・ 最近では新オピオイドの発売によってあまり使用されなくなったが,呼吸困難に対する効果があるとされるため,がん性リンパ管症などで呼吸困難がある患者に使用されることが多い.
3 )オキシコドン:徐放製剤,速放製剤,注射薬,TR 製剤
・ 1916 年から欧米には存在した.日本では 2002 年に発売されて以来,オピオイド鎮痛薬の第一選択肢として使用されている.現在,濫用防止製剤としてtamperresistan(TR)製剤が発売されている.
4 )タペンタドール:速放製剤,TR 製剤
・ タペンタドールはμ受容体作動作用とノルアドレナリン再取り込み阻害作用により鎮痛効果を発揮する,現在研究されているオピオイドの中では最新鋭のオピオイドである.その特性から一部神経障害性疼痛にも効果が期待されている.
・ 速放製剤はないため突出痛対策としては,他成分の速放製剤を使用する.
5 )フェンタニル:貼付製剤,口腔内崩壊錠
・ 合成麻薬であり麻酔領域で使用されて来た.脂溶性が高く,経皮吸収が可能なため,貼付剤として使用されることが多い.世界では 3 日間貼付剤しか発売されていないが,唯一日本だけに 1 日貼付製剤が発売されている.
・ フェンタニルは経口するとほぼすべてが肝臓で代謝されるため,内服薬はない.開始薬ではなく他のオピオイドからの変更が原則である.速放製剤としてRapidOnset Opioid である,口腔内崩壊錠が発売されている.
6 )メサドン
・ 世界的にはがん緩和医療におけるモルヒネの代替薬として重要性を増してきている.
・ 長時間作動性のμ受容体親和性と NMDA 受容体拮抗作用により鎮痛効果を発揮する.以前はメサドンの深刻な中毒性が報告されたため誤解を招き,がん疼痛治療における効果的な利用に障壁となっていた3).日本では開始薬ではなく,他のオピオイドからの変更が原則である.処方するにはe-learning による研修を修了しなくてはならない.
(3)専門的がん疼痛治療
・ ペインクリニックの技術の中でも神経ブロック療法と脊髄鎮痛法は数多くの患者の痛みの軽減に寄与する可能性があり,がん治療をする医師,緩和ケア関係者は必要があれば積極的に専門家に相談して適応を判断してもらうとよい.
1 )神経ブロック療法
・ オピオイド,鎮痛補助薬を使用しても,増量してもなかなか痛みが軽減しない,副作用のために鎮痛薬を増量できないなど,痛みの治療に難渋する患者に遭遇することは決して少なくない.その場合,痛みを伝えている神経をブロックすれば,痛みは軽減され,QOL は回復し,鎮痛薬の投与量も減量できる可能性がある4).
①神経ブロックの適応
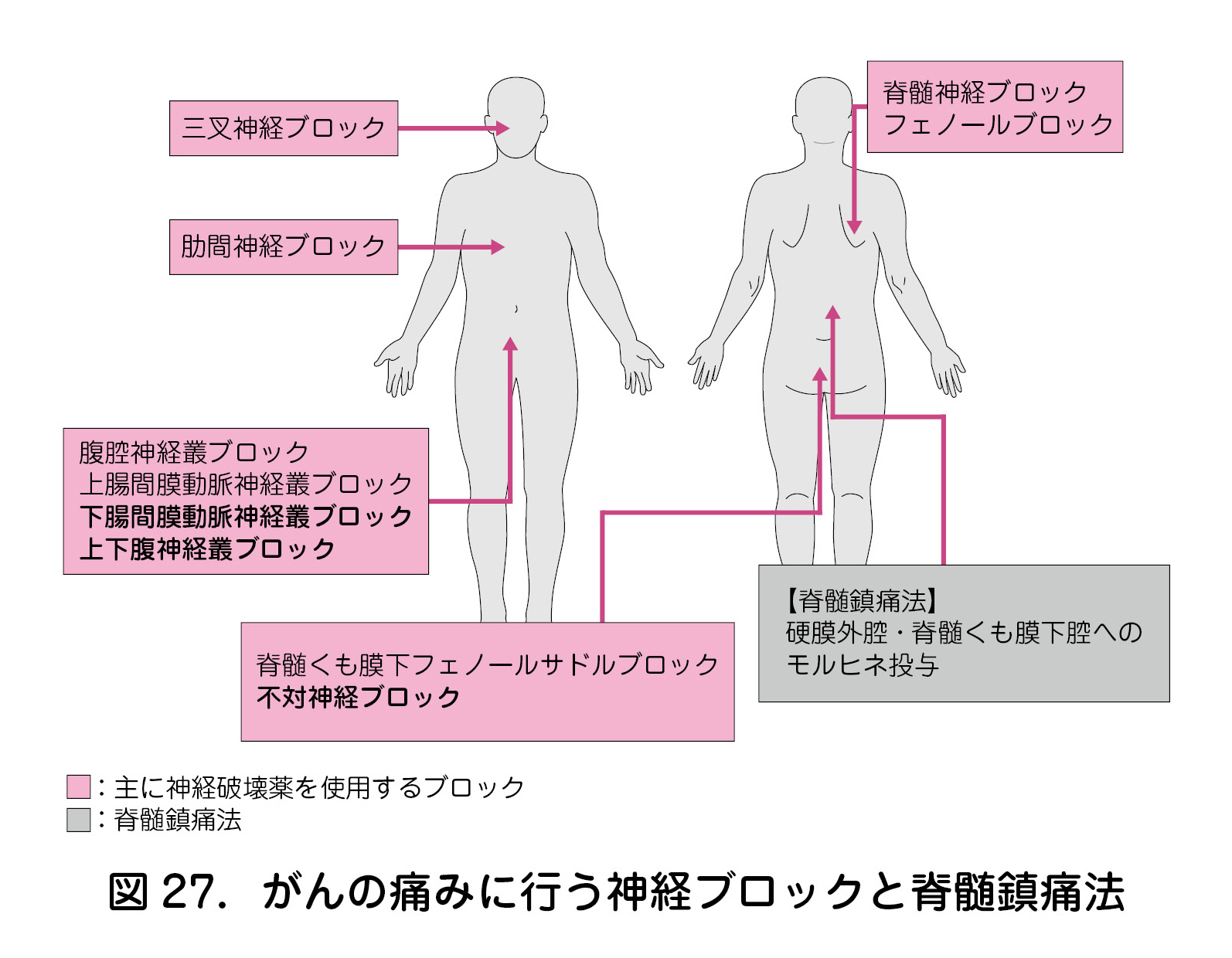
・ 図27 にがん疼痛治療で行うIntervention の一部を示す.
・ 痛みの部位,広さによって適応となる神経ブロックは様々であり,がん治療医や緩和ケア医ではなく専門家による適応判断が必要である.婦人科領域では,上下腹神経叢ブロックや不対神経節ブロック,そして脊髄鎮痛法が適応となることが多い.
②神経ブロックの種類
・ 神経ブロックは,大きく内臓痛に対する神経ブロックと脊髄神経系に対する神経ブロックとに分けることができる.
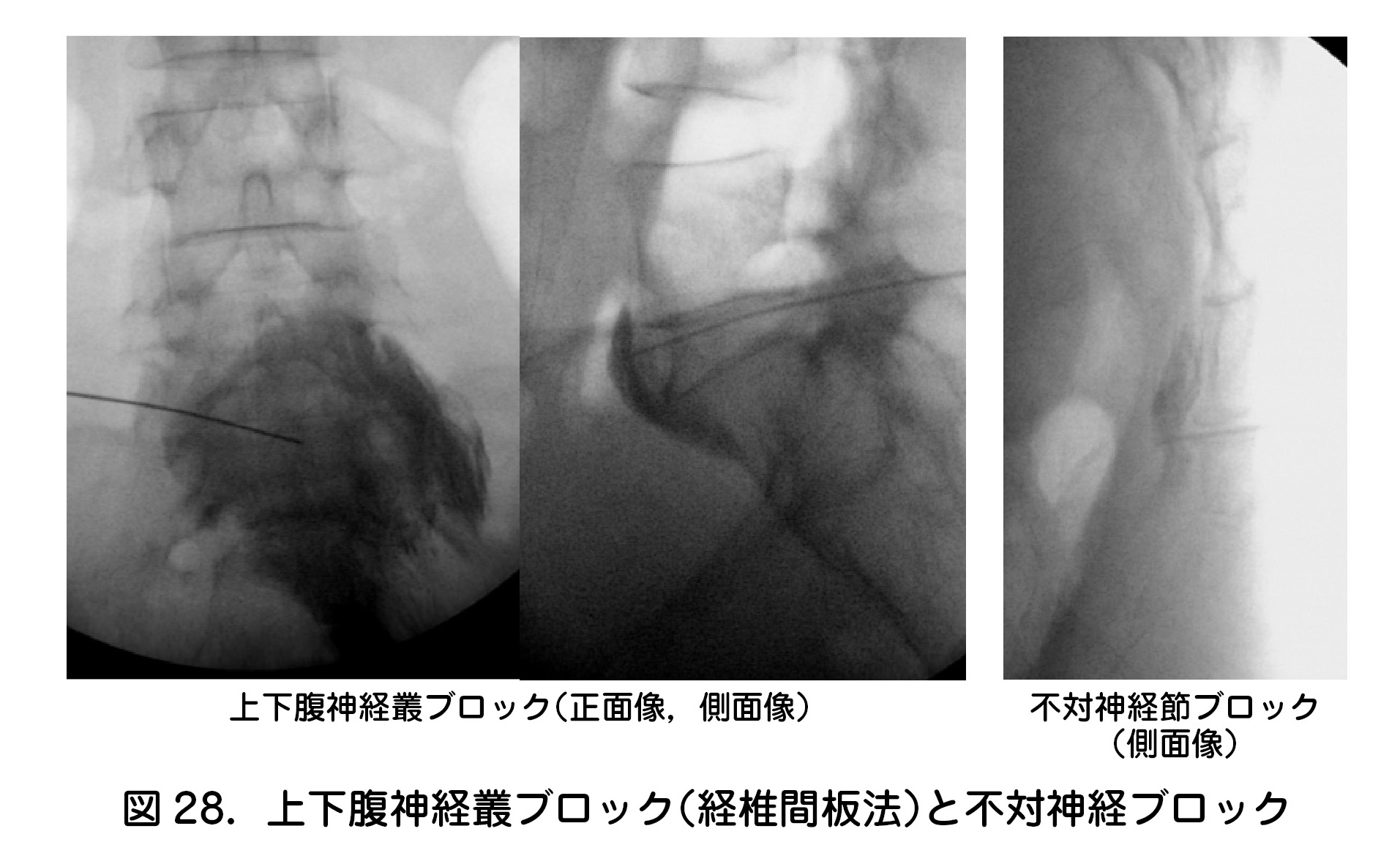
・ 腹膜播種,婦人科系悪性腫瘍,後腹膜腫瘍,骨盤内蔵腫瘍など腹部,下腹部,骨盤部の痛みでは,下腸間膜動脈神経叢ブロック,上下腹神経叢ブロックが適応となる(図28).
・ 肛門部,骨盤底部,会陰部の痛みに関しては不対神経ブロック(図28)が適応となることが多い.
・ Oliveira らの報告によると,内臓痛に対する神経ブロック(神経破壊)は患者の QOL を改善し,オピオイド使用量を減量させ,オピオイドによる副作用の軽減にも寄与するとしている5).
・ 脊髄神経系のブロックは,胸壁の浸潤,肋骨転移,胸壁の皮膚転移,肛門部痛,会陰部痛などで神経破壊の適応となる.頸部脊髄神経系,腰部脊髄神経系のブロックでは四肢の運動障害を来す可能性があるので神経破壊は実施しないことが多い.
・ 同領域の鎮痛が必要と判断した場合は,硬膜外鎮痛などの脊髄鎮痛法を選択する.
2 )脊髄鎮痛法
・ 脊髄後角における痛みの伝達の抑制をすることで痛みを軽減する方法.
・ 硬膜外腔鎮痛法と脊髄くも膜下腔鎮痛法の 2 つがある.
・ 1990 年代後半から 2005 年にかけて米国ではがん性疼痛管理に積極的に脊髄くも膜下鎮痛法が臨床使用されるようになり6),既に慢性疼痛へとその適用は拡がっている7).欧米先進国では,脊髄くも膜下鎮痛法は,内服で除痛困難ながん性疼痛に対する治療手段となっていると言ってもよい.
・ モルヒネを硬膜外腔に投与した場合は理論値ではあるが経口の約 20 倍,脊髄くも膜下腔に投与した場合は 200 倍と言われている8).
①硬膜外腔鎮痛法
・ オピオイドの増量では対処できない時,オピオイドの副作用などでそれ以上増量することができない時,そして主治医,本人,家族が同意した時に実施する9).激しい疼痛となった時の一時的回避手段としてもっとも有用である.
・ 薬液にはモルヒネと局所麻酔薬の混合液を使用し,機械型 PCA ポンプで痛みに応じて必要投与量を決めていく.
・ 硬膜外腔鎮痛が開始されると,痛みが急激に軽減し,使用していた全身投与オピオイドが相対的に過量となり,傾眠,呼吸抑制などの症状が出現することがあるので,全身投与量を速やかに減量する.
・ 臨床の現場では,硬膜外鎮痛で一時的に痛みが軽減している期間中に,神経ブロックを実施するか,脊髄くも膜下カテーテル留置にするかを検討していくことが多い.
②脊髄くも膜下腔鎮痛法
・ 脊髄くも膜下腔にモルヒネを使用すると硬膜外腔投与の 10 倍,内服の 200 倍の鎮痛効果が得られるとされている.硬膜外腔鎮痛法とは異なり脳脊髄液中に薬液を拡散させるため,濃度を調整した少用量の薬液量で済む.
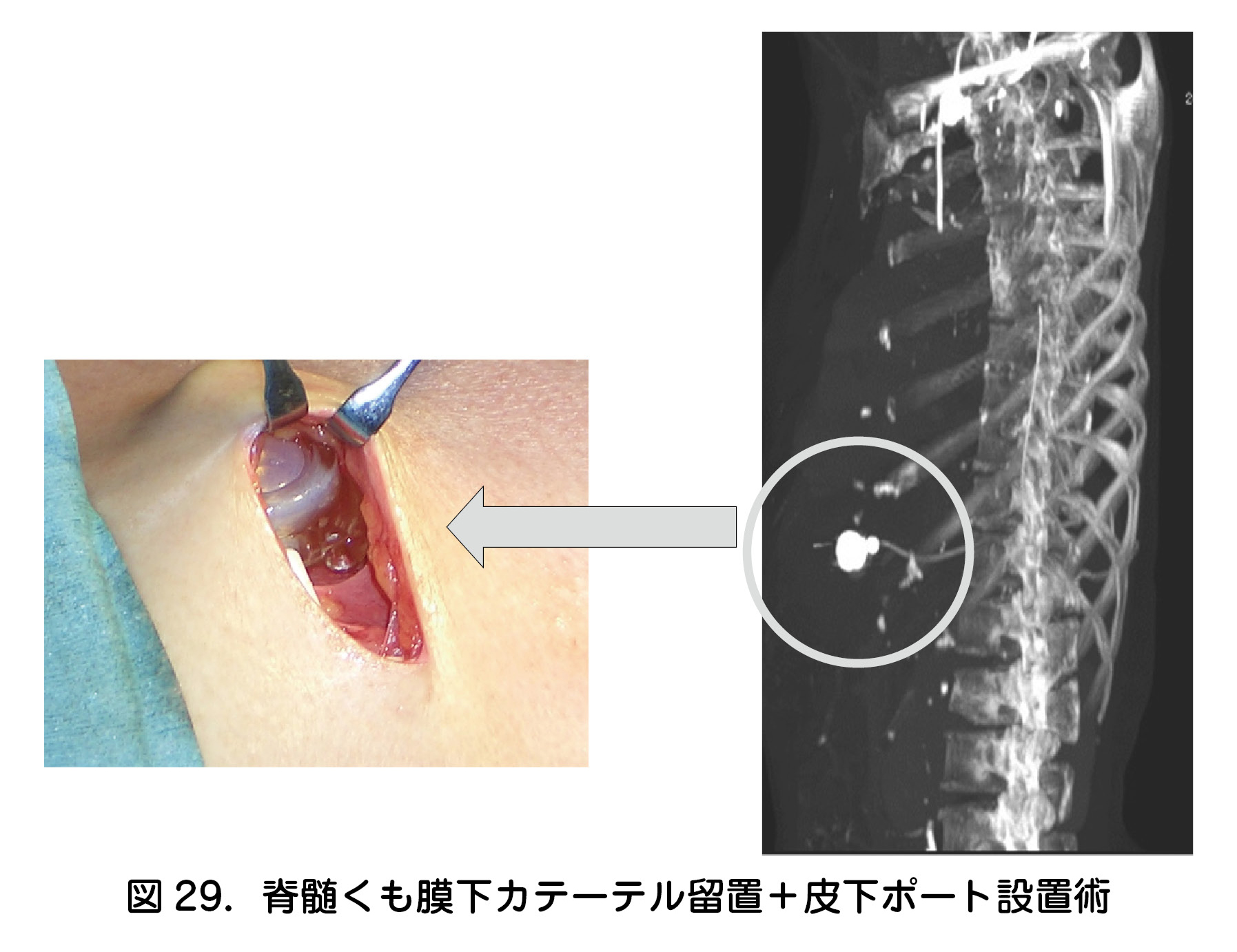
・ 硬膜外腔鎮痛法でコントロールができた後に在宅を目指した痛みの治療法として実施することもある.在宅へは感染,自己抜去,カテーテル切断などのリスクを最小限にする目的で,脊髄くも膜下カテーテルを埋め込み型ポートと接続する手術をしている(図29).
・ 合併症としてもっとも多いのは,硬膜穿刺後の頭痛である.年齢が若いほど発現リスクは高くなるが,通常は数日で改善することが多い.1 週間以上遷延する場合は,硬膜外 blood patch を実施することもある10).
文献
1) Cancer pain relief Second edition: With a guide to opioid availability, Word Health Organization, Geneva.
1996.
2) Zech DF, Grond S, Lynch J, et al. Validation of World Health Organization Guidelines for cancer pain relief:
a 10-year prospective study. Pain. 1995,63,65-76.
3)Symonds P. Methadone and the elderly. Br Med J. 1977, 1, 512.
4) Hattori S. Spinal analgesia and neurolysis. Textbook of Palliative Medicine and Supportive care, 2nd edition.
CRC press, Taylor & Farancis Group. edited by Bruera. Florida, USA. 2015, 449-460.
5) de Oliveira R, dos Reis MP, Prado WA. The effects of early or late neurolytic sympathetic plexus block on
the management of abdominal or pelvic cancer pain. Pain. 2004, 110, 400-408.
6)Lordon SP. Interventional approach to cancer pain. Curr Pain Headache Rep. 2002, 6, 202-206.
7) Bejjani GK, Karim NO, Tzortzidis F. Intrathecal granuloma after implantation of a morphine pump: case
report and review of the literature. Surg Neurol. 1997, 48, 288-291.
8) Dermot RF. Pain in malignant disease. Cancer pain: Management: Bonica’s management of Pain, third
edition, Lippincott Williams & Wilkins, Philadelphia, USA. 2001, 659-703.
9) Lema MJ, Invasive analgesia techniques for advanced cancer pain. Surg Oncol Clin N Am. 2001,10,127-
136.
10) Turnbull DK, Shepherd DB. Post-dural puncture headache: pathogenesis, prevention and treatment. Br J
Anaesth. 2003, 91, 718-729.





