(2)一般不妊治療
1)排卵障害に対する治療
ポイント
- 多囊胞性卵巣症候群における排卵誘発薬の第一選択薬は経口のクロミフェンやレトロゾールである.経口薬が奏功しない場合はFSH製剤を用いて低用量FSH漸増療法を行う.
- 高プロラクチン血症では,ドパミン作動薬のカベルゴリンが第一選択薬である.
①はじめに
- 排卵障害の原因は多岐にわたる.
- 鑑別すべき主な疾患は,①視床下部性排卵障害,②多囊胞性卵巣症候群,③早発卵巣不全,④高プロラクチン血症,⑤甲状腺機能異常の5つである.
- 本章では,日常臨床で遭遇する頻度が高い多囊胞性卵巣症候群と高プロラクチン血症について,治療手順を解説する.
②多囊胞性卵巣症候群(PCOS:polycystic ovary syndrome)
a.診断
- 多囊胞性卵巣症候群は,月経異常や不妊,男性化,肥満,インスリン抵抗性など,多彩な症状を呈する症候群で,排卵障害の70~80%を占める.
- 日本では,①無月経・希発月経・無排卵周期症などの月経周期異常,②超音波検査で両側卵巣に多数の小卵胞または抗ミュラー管ホルモン(AMH:anti-Müllerian hormone)高値,③アンドロゲン過剰症(血中総テストステロン高値またはアンドロゲン過剰症状)またはLH高値,の3つすべてを満たす場合を,PCOSと診断する(23頁表5参照).
- 日本では,男性化徴候を呈するような肥満型PCOS(BMI≧25)は少なく,肥満を伴わないPCOS(非肥満型PCOS,BMI<25)が7割以上を占める.非肥満型PCOSでは,LH高値がより顕著である(図13).
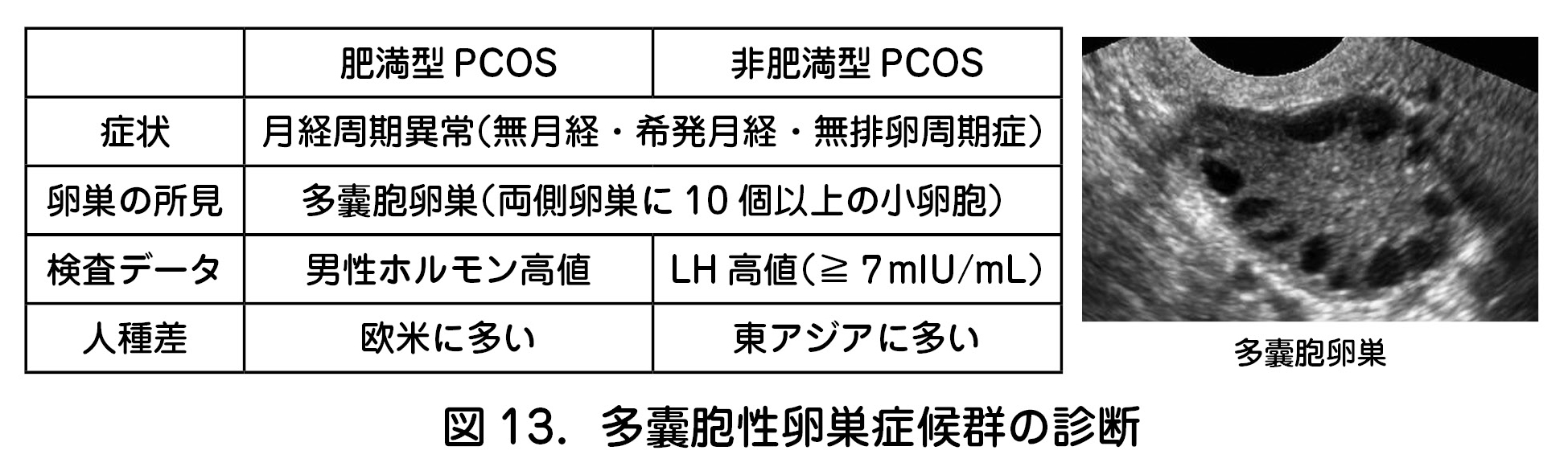
b.治療(図14)
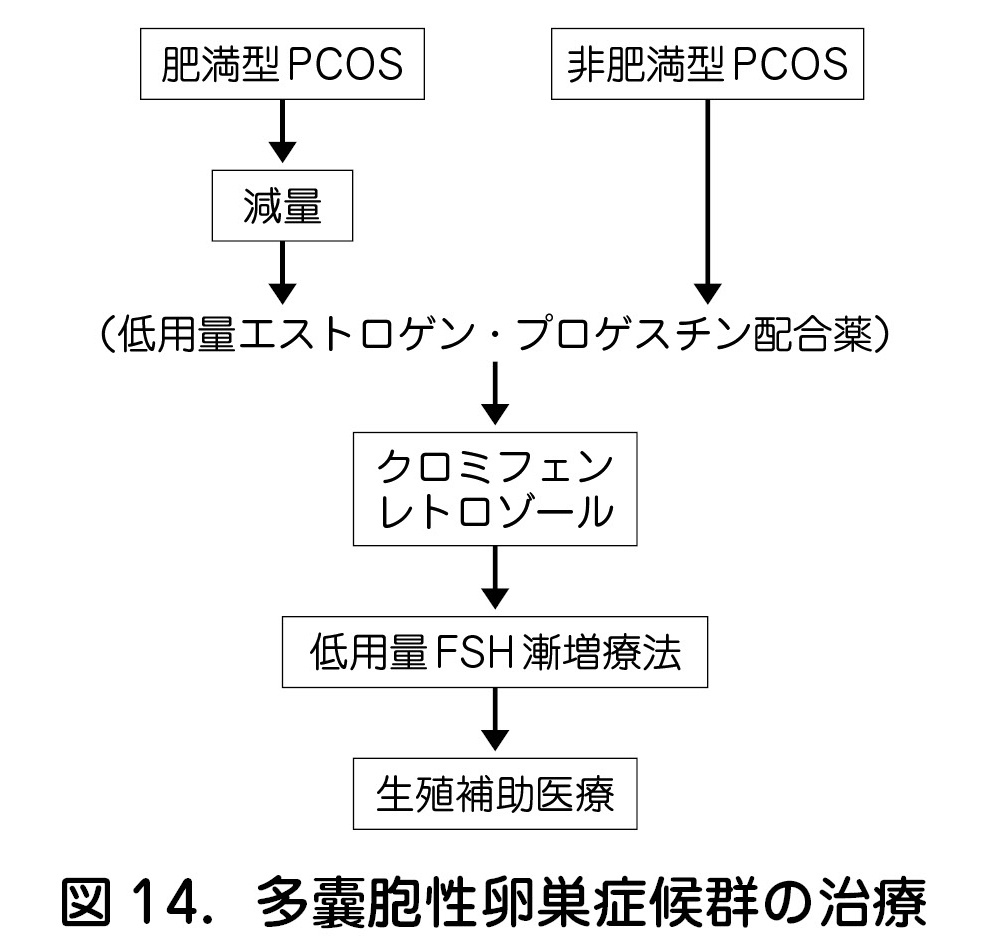
- 肥満型PCOSでは,食事制限や運動により,5~10%の減量を目指す.減量が成功すると,高アンドロゲン状態は改善し,排卵誘発への反応性も回復する.ただし35~37歳以上のPCOS症例に対し,減量に多くの時間を費やすのは得策でない.
- 排卵誘発の前に,低用量エストロゲン・プロゲスチン配合薬を1~2周期投与し,高アンドロゲン状態や高LH状態の改善を図ることがある.
- 日本において,PCOSに対する排卵誘発の第一選択薬は,クロミフェンである.クロミフェン周期ではLHサージが発現しづらいので,hCG製剤を注射して排卵を誘導する.クロミフェンは,排卵率が高い割に妊娠率が低く,頸管粘液や子宮内膜への悪影響が懸念されている.
- アロマターゼ阻害薬(レトロゾール)の排卵率や生児獲得率が,クロミフェンに勝ることから,海外ではレトロゾールが排卵誘発の第一選択とされている.近年,日本でもレトロゾールが保険適用化(適応は,生殖補助医療における調節卵巣刺激,多囊胞性卵巣症候群における排卵誘発,原因不明不妊における排卵誘発)されており,今後はクロミフェンからのシフトも予想される.以前レトロゾールの催奇形性が懸念されたこともあったが,現在は否定的である.
- 耐糖能異常を有する肥満型PCOSにおいて,クロミフェンによる排卵誘発が奏功しない場合,インスリン抵抗性改善薬(メトホルミン)の併用が考慮される.しかしながら,メトホルミンは排卵率と妊娠率を向上させるものの,生児獲得率を改善しないことから,その治療効果は限定的とされている.
- 経口の排卵誘発剤が奏功しない場合,低用量FSH漸増療法が適応になる.実際には,月経3~4日目から連日FSH製剤50~75単位を自己皮下注射し,5~6日おきに卵胞発育をモニタリングしながら,主席卵胞の発育状況に応じて50%ずつ増量していく(例:50単位→75単位→100単位→150単位→225単位).
- いずれの排卵誘発法でも,排卵のトリガーとしてhCG製剤の注射を用いる.ただし,16mm以上の発育卵胞を4個以上認める場合は,多胎妊娠や卵巣過剰刺激症候群の発症リスクが高く,hCG製剤をキャンセルすべきである.
③高プロラクチン血症
a.診断
- 高プロラクチン血症は,排卵障害の5~10%を占める.高プロラクチン血症では,視床下部のGnRHパルス分泌や下垂体由来のLHサージが阻害されるため,排卵が抑制される
- 月経異常や乳汁漏出を認める場合は,血中プロラクチン(PRL)濃度を測定する.検査のタイミングは,月経期や卵胞期が望ましく,排卵期や黄体期を避ける.
- 血中PRL濃度≧30ng/mLの場合を,高プロラクチン血症と診断する.血中PRL濃度≧100ng/mLの場合は,プロラクチン産生下垂体腫瘍(プロラクチノーマ)の可能性があり,頭部MRI検査を行う.
- プロラクチン放出因子として甲状腺刺激ホルモン放出ホルモン(TRH),プロラクチン阻害因子としてドパミンが知られている.高プロラクチン血症を認めた場合,甲状腺機能低下が原因のことがあるので,TSH,fT3,fT4など甲状腺機能を追加検査する.
- 精神科や消化器系の薬剤が,高プロラクチン血症を来すこともある.特にスルピリドやH2受容体拮抗薬,メトクロプラミド,SSR(I選択的セロトニン再取込阻害薬),SNR(Iセロトニン・ノルアドレナリン再取込阻害薬),エストロゲン製剤(経口避妊薬を含む)の服薬歴に注意する.
b.治療
- ドパミン作動薬(カベルゴリン,ブロモクリプチン,テルグリド)が第一選択である.
- カベルゴリンは半減期が長く,コンプライアンスのよい薬剤である.週1回(同一曜日)の就寝前に,0.25mg/回から開始し,少なくとも2週間以上の間隔で0.25mg/回ずつ増量する.一般的な維持量は0.25~0.75mg/回で,上限は1mg/回である.
- ブロモクリプチンは,毎夕食後に2.5mg/日から開始する.一般的な維持量は2.5~7.5mg/日である.眠前に服用することで,嘔気・嘔吐といった副作用がやや緩和される.
- テルグリドは,毎夕食後に0.5mg/日から開始する.ブロモクリプチンと比べて,嘔気・嘔吐は軽度である.
- 妊娠が成立したらドパミン作動薬を休薬する.不育症におけるドパミン作動薬の流産予防効果は,限定的とされている.
- プロラクチノーマの場合も,第一選択はドパミン作動薬だが,薬物療法が奏功しないケースは手術が適応になる.
2)排卵誘発法
ポイント
- 単一卵胞の発育を目指し,排卵障害の原因に合わせた排卵誘発法を選択する.
- 成熟卵胞(卵胞径16mm以上)4個以上では,多胎妊娠の防止のためにhCG製剤の投与をキャンセルする.
①排卵誘発の対象
- 排卵誘発の対象は下記である.
- 排卵障害を認める不妊女性に対する排卵誘発(OI:ovulation induction)
- 排卵を認めるが卵胞発育不全および黄体機能不全を呈するもの,
あるいは稀発月経などに対する卵巣刺激(OS:ovarian stimulation) - 原因不明不妊症
②病態に応じた排卵誘発法
- 単一卵胞の発育を目指し,排卵障害の原因に合わせた排卵誘発法を選択する.
a.多囊胞性卵巣症候群(PCOS:polycystic ovary syndrome)
PCOS患者に対する治療方針の基本は,インスリン抵抗性の増悪因子である肥満を改善することである.すなわち肥満(BMI25㎏/m2以上)であれば減量を指示することが最も重要である.次いで薬物療法としては従来クロミフェン療法が第一選択であったが,アロマターゼ阻害薬であるレトロゾールの優位性が示されている.近年ではインスリン抵抗性改善薬であるメトホルミンがPCOS患者の排卵障害に有効であることが報告されており,挙児希望のPCOS症例に用いられるが,肥満,耐糖能異常またはインスリン抵抗性を有する患者を適応とする1).
b.卵巣性排卵障害
持続的な高FSH血症はFSHへの感受性を低下させるため,一般的にはクロミフェンおよびゴナドトロピン製剤を使用しても卵胞が発育しないことが多い.この場合,カウフマン療法(E+P製剤),エストロゲン療法により血中FSHまたはLHの値を低下させ,引き続きゴナドトロピン療法を行うと,稀に奏効することがある.
c.高プロラクチン血症
プロラクチノーマあるいは原因疾患の鑑別を行った上で,ドパミン作動薬であるカベルゴリンの内服を検討する.プロラクチン産生腫瘍によるForbes-Albright症候群にはドパミン作動薬あるいは外科的治療の選択肢を考慮する.一般的には径1㎝未満のマイクロアデノーマで乳汁漏出以外の自覚症状がない場合はドパミン作動薬を投与し,径1㎝以上のマクロアデノーマで症状を伴うものであれば手術適応について脳神経外科にコンサルトする.精神科疾患および消化器疾患に対する継続的な服薬が必要な薬剤性高プロラクチン血症であれば,薬剤の中止および減量が可能かどうかを担当医と相談する.
特発性の高プロラクチン血症に対してはドパミン作動薬を選択するが,それでも排卵を確立できない場合はクロミフェン療法の併用を試みる.
d.中枢性卵胞発育不全
LHおよびFSHの基礎値が低値を示す.コントロールが難しいため,基本はLHおよびFSH両方の成分を含むhMG製剤の使用を考慮する.下垂体からのLHの部分的な分泌を認める症例では,適宜rFSH(リコンビナント)製剤の使用を考慮する.
e.機能性卵胞発育不全
LHおよびFSHの基礎値は正常であるにもかかわらず,卵胞が発育しない病態である.比較的軽症の視床下部障害がこれに含まれる.クロミフェンあるいはゴナドトロピン製剤で刺激すると卵胞発育が得られることが多い.
f.原因不明不妊症
原因不明不妊に対して行う排卵誘発法の有効性については,明らかなエビデンスはない.人工授精と併用してクロミフェンあるいはゴナドトロピン療法を選択することで妊娠率を向上できるが多胎率の上昇が懸念され2),ゴナドトロピン療法を積極的に勧めるよりは体外受精を勧めた方がよいとの意見もある.患者の希望,費用およびリスクも考慮の上で施行するのが望ましい.
③薬剤別処方例
- 多胎妊娠の防止のために,成熟卵胞(卵胞径16mm以上)4個以上ではhCG製剤の投与をキャンセルする.
a.クロミフェン療法:クロミフェンクエン酸塩(CC:Clomifenecitrate)
月経5日目から1日50mg,5日間の内服から開始し,無効な場合は100mg,5日間に増量する.排卵は投与終了後,通常7~10日後に起こることが多く,排卵時の卵胞径は自然周期よりも大きくなる傾向がある.
数周期にわたり連用する場合,抗エストロゲン作用により子宮頸管粘液の減少および子宮内膜の菲薄化による月経量の減少を訴えることも多い.連続してクロミフェンを使用した場合は,休薬することで上記副作用は回復する.
【処方例】クロミッド®(セロフェン®)錠(50mg) 開始量1回1錠 1日1回
食後5日間,月経5日目より開始(1日2錠まで増量可能)
b.シクロフェニル療法
クロミフェンと同様に視床下部~下垂体系に作用してGnRHおよびゴナドトロピンの分泌を促進する.排卵誘発効果は50%前後とクロミフェンより低いものの,頸管粘液の減少や子宮内膜の菲薄化を生じることが少ないのが特徴である.比較的軽度の排卵障害に対して第一選択薬となる.
【処方例】セキソビット®錠(100mg)開始量1回2錠 1日2回 食後5日間,
月経5日目より開始(1日6錠まで増量可能)
c.ドパミン作動薬
高プロラクチン血症に対して手術適応となるプロラクチノーマ以外では薬物療法が第一選択である.ドパミン作動薬であるブロモクリプチン,テルグリド,あるいはカベルゴリンが用いられている.ブロモクリプチンは嘔気嘔吐の副作用が強く,1.5~2.5mgから開始し,プロラクチンが正常化する維持量(5.0~7.5mg)まで漸増する.テルグリドはブロモクリプチンより消化器症状が軽微である.0.5mg/日から開始し,0.5~1.0mgで調節する.超長時間作用型で消化器症状の副作用が少ないカベルゴリンは,最少量から開始し,2週間以上の間隔で血清プロラクチン値をモニターしながら0.25~0.75mg/週を維持量として投与量を増減する.カベルゴリンは副作用も少なく服薬コンプライアンスにも優れるため,近年選択されることが多い.胎盤通過性があるため,妊娠成立後は原則としては服薬を中止する.
【処方例】カバサール®0.25mg1回1錠食後週1回投与で開始.
最大量は1回1mgまで.
d.ゴナドトロピン療法
PCOS症例に対してはLHの投与を最小限に留めるため,FSHあるいはrFSH製剤を第一選択とする.コンプライアンスの面からは,自己注射可能な製剤を用いることが可能となっているrFSH製剤が有用である.
【処方例】ゴナールF®75単位/日 皮下注(自己注射可能)連日投与
月経周期2~5日目より開始通常7~10日間投与する.
卵胞発育をモニターし反応性が悪い場合
(主席卵胞10mm未満)は初期投与量の半量を増量していく.
主席卵胞が18mm以上に到達した時点でhCG製剤5,000単位を投与する.
文献
- 1)生殖・内分泌委員会報告「本邦における多囊胞性卵巣症候群の治療法に関する治療指針作成のための小委員会」報告.日本産科婦人科学会雑誌 61: 902-912, 2009
- 2)Ayeleke RO, et al. Intra-uterine insemination for unexplained subfertility. Cochrane Databases Syst Rev. 3(3): CD001838, 2020
3)卵管因子に対する治療
ポイント
- 卵管因子を引き起こす原因にクラミジア感染症,子宮内膜症がある.
- 子宮卵管造影検査は卵管の疎通性を確認するために重要な検査である.ただし造影検査前の感染症の有無,甲状腺機能の評価は重要である.
- 卵管水腫は体外受精の成績を低下させる可能性があり,卵管摘出術などを考慮することがある.
卵管因子は女性の不妊症原因の30~40%とされており,治療を行う上で,原因疾患,検査方法,治療方針を理解することは重要である.当然ながら,卵管病変以外にも患者年齢,卵巣予備能,既往妊娠の有無,ほかの不妊因子の有無を勘案して治療方針を立てることになる.
①卵管因子を起こす疾患
卵管因子を引き起こす疾患:クラミジア感染症,子宮内膜症が主な疾患である.ほかに異所性妊娠,開腹手術の既往などが挙げられる.
a.クラミジア・トラコマチス(クラミジア)
クラミジア抗原検査では,核酸増幅検査(PCR法:polymerase chain reaction)が感度,特異度ともに高く,現行感染の診断には第一選択となる1).PCR法の登場前には抗体検査が主に用いられてきた.抗体価が高値になるにつれ卵管周囲癒着スコアと関連するという報告もあることから,不妊症の観点からはクラミジア抗体価検査も意義が残っている1).
b.子宮内膜症
卵管性不妊を引き起こす可能性があり,腹腔鏡手術での検査を行う(後述).
②検査方法
検査方法としては,子宮卵管造影,超音波下子宮卵管造影,子宮鏡下選択的通水検査,腹腔鏡手術による評価が挙げられる.
a.子宮卵管造影(HSG:hysterosalpingography)
HSGは卵管評価に有用であるが,卵管通過性の感度は0.65,特異度は0.83であり,卵管疎通性の診断には限界があることが知られている2).
ア 甲状腺への影響
HSG検査時に用いられるヨード含有造影剤には水溶性(イソビスト®)と油性(リピオドール®)がある.過剰なヨード摂取により一過性に甲状腺ホルモン合成が低下することがあり,HSG検査後甲状腺機能には留意する必要がある.油性造影剤群では検査後,約25%の女性が血中TSH(甲状腺刺激ホルモン)の上昇,甲状腺ホルモン(freeT4)は正常を示す,いわゆる潜在性甲状腺機能低下症を呈した.一方,水溶性造影剤群では10%弱の症例に潜在性甲状腺機能低下症を認めたとの報告がある3).HSG検査後の甲状腺の反応を予測する意味でも検査前の甲状腺機能評価は重要である.
イ HSG検査後の妊娠率について
最近の話題として油性造影剤をHSGに用いた場合,その後に妊娠するケースが水溶性造影剤との比較し,オッズ比で1.374)や1.675)と有意に上昇するという報告がある.ただし,これら論文の対象症例は内分泌的な障害がなく,卵管の病理学的リスクが低い症例を対象にした報告であり,不妊女性に一般化される知見でないことは留意すべきである.特に,卵管水腫症例では,長期間,体内にヨードが残存することとなる.
b.超音波下子宮卵管造影(HyCoSy:hysterosalpingo-contrast sonography)
放射線被爆のリスクがなく,甲状腺機能への影響もなく検査を行うことができる点で有用である.現時点ではフェムビュー®が使用可能であるが,保険適用外であり,また,静止画像での疎通性の確認が困難であるため,施行者の技術に依存する部分が多い.
c.子宮鏡下選択通水検査
軟性子宮鏡下に2Frのカテーテル(例:キタザトEDSカテーテル®)を各卵管口へ約1㎝程度挿入し,希釈インジコカルミン液を注入し,子宮内腔に逆流する場合,閉塞を推定する.一方で10mLを挿入しても子宮内腔への逆流を認めず,超音波断層法検査で骨盤内への液体貯留を確認できた場合は,疎通性があると判断する6).
d.腹腔鏡検査
特に子宮内膜症では卵管が重要であり,EFI(endometriosis fertility index)スコアの評価を行い術後ARTへの移行など方針を立てる上でも腹腔鏡検査は有用である7).『日本産婦人科医会研修ノートNo.102子宮内膜症・子宮腺筋症』を参照.
③治療
卵管鏡下卵管形成術(FT:fallopian tuboplasty),体外受精が主体となる.卵管に液体貯留が続く,いわゆる卵管水腫の状態では着床率が低下することがいわれており,妊娠に至らない場合は,卵管切除術などを考慮することになる(図15)8).
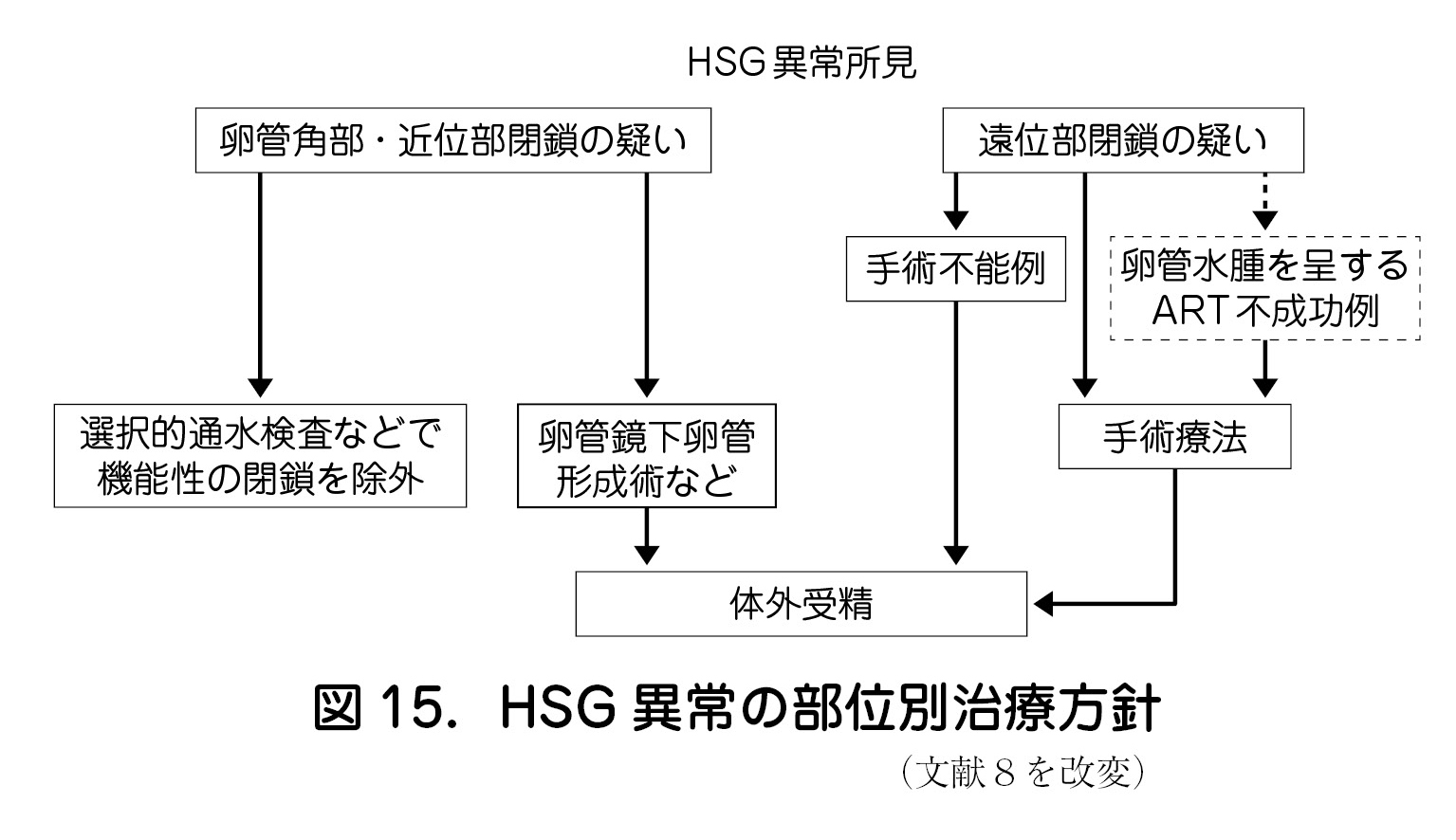
a.部位別治療方針
ア 卵管角部閉鎖
器質的な異常がないにもかかわらず,卵管角部閉鎖が疑われた場合,子宮卵管口の攣縮など一時的である可能性もあることから,再検査や子宮鏡下選択的卵管通水検査を試みることが勧められる.
イ 卵管近位部閉鎖
FTは検討されるべきある.FT後の妊娠率は約30%との報告がある9).本手術は術後半年程度の体外受精以外の妊娠を期待して経過をみるため,時間的余裕が残された37歳程度までを対象年齢とすることが多い.ただし,体外受精を望まない症例には特に年齢の制限はないと思われる6).
ウ 卵管遠位部閉鎖
軽度
限定的なフィルム状の癒着や軽度の卵管留水症病変は予後良好であり,癒着剝離や卵管開口・卵管采形成術により妊娠率向上を望むことができる10).
卵管開口・卵管采形成術(Bruhat法):卵管采側の卵管口を広げ,反転させ,卵管漿膜と縫合し固定する8).
重度
卵管の強固な癒着,卵管壁が薄くなるほどの卵管拡張,卵管粘膜の欠損・欠如症例では卵管の修復が困難であり,卵管切除の適応となり,体外受精が必要となる.
b.卵管留水症を有する体外受精不成功例に対して
子宮内腔への卵管内容液の流入による受精卵への直接的な影響,子宮内膜受容能の低下が想定される11).超音波断層法検査で卵管腫大を認めるような液体貯留は,妊娠への影響が大きく手術が考慮される.
ア 卵管切除術
メタアナリシスにより,卵管留水症を有する女性は体外受精前に卵管切除あるいは卵管閉鎖術を考慮すべきと示されている12).片側症例であっても,手術により体外受精の成績が向上することが報告されている.卵管切除術では,卵巣への血流を可能な限り保つために卵管に近い部位での切除が望まれる13).
イ 卵管開口術
卵管留水症に対して体外受精前に開口術により妊娠率が改善することが示されている11)が再閉鎖の可能性には留意すべきである.
ウ 卵管閉鎖術
人工的に近位卵管をバイポーラー電極やクリッピングを用いて閉鎖を行う.同処置は卵管切除よりも術後のFSH上昇を抑えたという報告がある14).ただし,卵管水腫症の増大や卵管癌を含めた病理的評価ができないことが危惧される.
文献
- 1)野口靖之,坂井啓造.性器クラミジア感染症,産科と婦人科増刊号.診断と治療社.87:348-351,2020
- 2)Swart P, Mol B W J, Van der Veen F, Van Beurden M, Redekop W K, Bossuyt P M M. The Accuracy of Hysterosalpingography in the Diagnosis of Tubal Pathology: A Meta-Analysis. Fertil Steril. 64: 486-491, 1995
- 3)So S, Yamaguchi W, Tajima H, Nakayama T, Tamura N, Kanayama N, Tawara F. The Effect of Oil and Water-Soluble Contrast Medium in Hysterosalpingography on Thyroid Function. Gynecol Endocrinol. 33: 682-685, 2017
- 4)Dreyer K, van Rijswijk J, Mijatovic V, Goddijn M, Verhoeve H R, van Rooij I A J, Hoek A, Bourdrez P, Nap A W, Rijnsaardt-Lukassen H G M, et al. Oil-Based or Water-Based Contrast for Hysterosalpingography in Infertile Women. N Engl J Med. 376: 2043-2052, 2017
- 5)Wang R, van Welie N, van Rijswijk J, Johnson N P, Norman R J, Dreyer K, Mijatovic V, Mol B W. Effectiveness on Fertility Outcome of Tubal Flushing with Different Contrast Media: Systematic Review and Network Meta-Analysis. Ultrasound Obstet Gynecol. 54: 172-181, 2019
- 6)田島博人.子宮鏡下選択的通水と卵管鏡下卵管形成術,臨床婦人科産科 増刊号.76(4):202-205,2022
- 7)Adamson G D, Pasta D J. Endometriosis Fertility Index: The New, Validated Endometriosis Staging System. Fertil Steril. 94: 1609-1615, 2010
- 8)日本産科婦人科学会,日本産婦人科医会編.CQ315 子宮卵管造影所見からみた卵管病変の取り扱いは?, 産婦人科診療ガイドライン婦人科外来編2017 年版
- 9)Sueoka K, Asada H, Tsuchiya S, Kobayashi N, Kuroshima M, Yoshimura Y. Falloposcopic Tuboplasty for Bilateral Tubal Occlusion. A Novel Infertility Treatment as an Alternative for in-Vitro Fertilization?. Hum Reprod. 13: 71-74, 1998
- 10)Nackley A C, Muasher S J. The Significance of Hydrosalpinx in in Vitro Fertilization. Fertil Steril. 69: 373- 384, 1998
- 11)Salpingectomy for Hydrosalpinx Prior to in Vitro Fertilization. Fertil Steril. 90, 2008 12)Johnson N, van Voorst S, Sowter M C, Strandell A, Mol B W J. Surgical Treatment for Tubal Disease in Women Due to Undergo in Vitro Fertilisation. Cochrane Database Syst Rev 2010. 2010
- 13)Chan C C W, Ng E H Y, Li C F, Ho P C. Impaired Ovarian Blood Flow and Reduced Antral Follicle Count Following Laparoscopic Salpingectomy for Ectopic Pregnancy. Hum Reprod. 18: 2175-2180, 2003
- 14)Nakagawa K, Ohgi S, Nakashima A, Horikawa T, Irahara M, Saito H. Laparoscopic Proximal Tubal Division Can Preserve Ovarian Reserve for Infertility Patients with Hydrosalpinges. J Obstet Gynaecol Res. 34: 1037-1042, 2008
4)子宮因子に対する治療
ポイント
- 不正出血などの症状だけでなく,着床障害の原因になっているかどうかが重要である.
- ホルモン治療は投与終了後に病変が投与前の状態に戻るため,挙児希望のある患者に対しては基本的には治療とならない.
①粘膜下子宮筋腫
子宮鏡検査やソノヒステログラフィで,粘膜下子宮筋腫の大きさ,子宮内腔への突出率,漿膜面との距離が評価される.通常,過多月経や貧血といった症状があれば治療対象となるが,挙児希望の場合は着床障害の原因になると考えられれば治療対象となる.
治療
- ホルモン治療:GnRHアナログ製剤は6カ月間のみ投与可能である.投与終了後は投与前の状態に戻るため,挙児希望があるような非閉経期の女性には根治的治療にならない.
- 手術:根治的には子宮摘出術であるが,挙児希望のある場合は子宮筋腫核出術となる.子宮筋腫核出術を子宮鏡下,腹腔鏡下,腹腔鏡補助下あるいは開腹で行うかは,子宮筋腫の数・大きさ・内腔への突出率・子宮筋腫漿膜間距離を踏まえ,施設ごとの選択となる.『産婦人科診療ガイドライン婦人科外来編2023』では子宮鏡下子宮筋腫核出術は子宮筋腫径が30mm以下かつ突出度が50%以上を目安とし,特に優れた術者ではこの限りではないとしている.術前にGnRHアナログ製剤を用いることで,子宮筋腫の縮小と術中出血量の減少が期待できるが,正常筋層も薄くなるため子宮筋腫漿膜間距離が投与前と変化することに注意を要する.術後の子宮内腔癒着を予防するために,主に子宮内膜の欠損が広い症例に対して,術直後から術後の月経が2~3回終了するまでintrauterine device(IUD)(FD-1)挿入を行ったり(保険適用外),カウフマン療法を行ったりする.また,second look 子宮鏡を術後月経2~3回終了後に行う.
②子宮内膜ポリープ
大きさなどより病理診断が必要な場合,着床障害の原因になると考えられた場合,症状(不正出血,過多月経など)の原因になっていると考えられた場合に治療対象となる.
治療
- 子宮鏡下子宮内膜ポリープ摘出術あるいは子宮内膜全面掻爬術となる.ポリープの取り残しや,それによる再発,症状の再燃を防ぐために子宮鏡下に行うことが望ましい1).
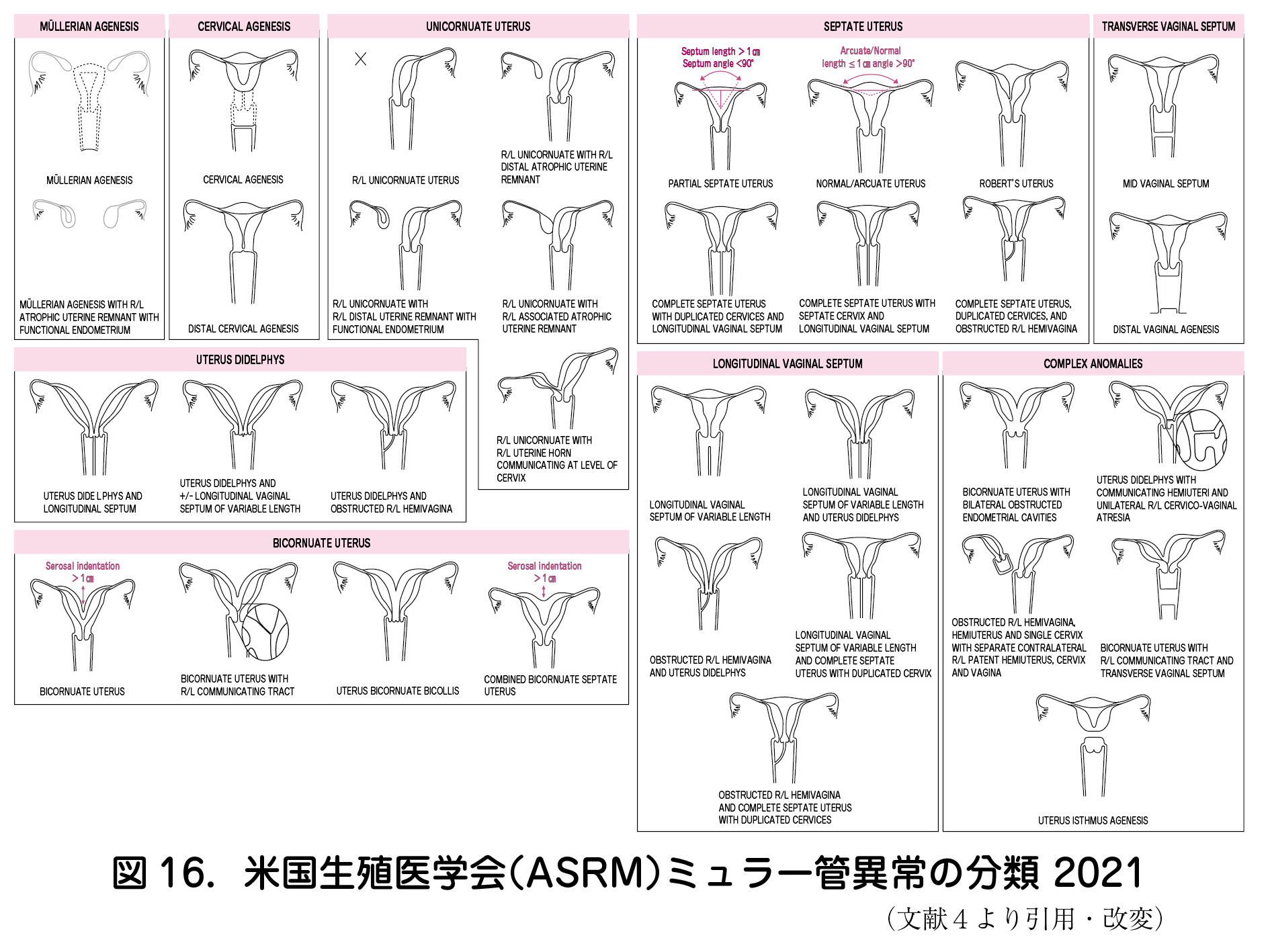
③子宮形態異常(図16)
Chanらの報告によれば,中隔子宮は,妊娠率を減少させ,初期流産率と早産率を上昇させる.双角子宮,重複子宮,単角子宮は妊娠率を減少させないが,早産率は上昇させる.双角子宮は初期および中期流産率を,単角子宮は初期流産率を上昇させる.弓状子宮は中期流産と関連している2).
治療
- 機能性子宮内膜を伴わない子宮形態異常については,理論的には子宮移植あるいは代理母が治療法となるが,代理母は日本では認められていない.
- 子宮頸部無形成の場合,子宮開口術を行う.ただし,合併している子宮内膜症のために生殖補助医療が必要になることが多いと報告されている3).
- 中隔子宮に対して子宮鏡下子宮中隔切除術で妊娠率が改善する可能性が示唆されているが,手術は広くは受け入れられていない.子宮形態異常に対して手術を行った場合の無作為割り付け試験は行われておらず,不妊や流産の原因だと判断された場合のみ,手術療法を行うことが考慮される.
④帝王切開瘢痕部症候群(cesarean scar disorder)
帝王切開後に創部筋層の楔状の解剖学的変化が生じることが特徴とされており,月経異常,月経困難症,続発性不妊症などの臨床症状に加えて,瘢痕創部筋層の菲薄化の画像所見や子宮鏡検査で帝王切開瘢痕創部に病巣を確認することで,診断をする.
治療
- ホルモン治療:保険適用にはなっていないが,低用量エストロゲン・プロゲスチン配合薬5),子宮内黄体ホルモン放出システム6)の有効性が報告されており,プロゲスチン製剤やGnRHアナログ製剤の効果も期待される.投与中止後は投与前の状態に戻るので,挙児希望のある女性は対象外である.
- 手術:瘢痕部病巣の切除は子宮鏡下で実施可能であるが,瘢痕創部筋層の厚さによって腹腔鏡(あるいは開腹)で監視下あるいは同時に用いての子宮鏡手術が望ましい.子宮鏡下手術を安全に行うのに必要な瘢痕創部筋層の厚さは2.5~4mmと様々な報告があるが,確立したものはない.術前にGnRHアナログ製剤を長期間投与すると術中に病巣の確認が困難になるため注意を要する.帝王切開創子宮瘢痕部を原因とする続発性不妊症,過長月経,器質性月経困難症に対して実施した場合にのみ腹腔鏡下子宮瘢痕部修復術を算定できる.
⑤Asherman症候群
着床障害の原因になるため,子宮鏡下子宮内腔癒着剝離術を行う.
文献
- 1)Preutthipan S, et al. Hysteroscopic polypectomy in 240 premenopausal and postmenopausal women. Fertil Steril. 83: 705-709, 2005
- 2)Chan YY, et al. Reproductive outcomes in women with congenital uterine anomalies: a systematic review. Ultrasound Obstet Gynecol. 38: 371-382, 2011
- 3)Fedele F, et al. Reconstructive surgery for congenital atresia of the uterine cervix: a systematic review. Arch Gynecol Obstet. 2022
- 4)Pfeifer SM, et al. ASRM müllerian anomalies classification 2021. Fertil Steril. 116: 1238-1252, 2021
- 5)Tahara M. Preliminary report of treatment with oral contraceptive pills for intermenstrual vaginal bleeding secondary to a cesarean section scar. Fertil Steril. 86(2): 477-479, 2006
- 6)Chen Y, et al. Preliminary report on the use of a levonorgestrel intrauterine system for the treatment of intermenstrual bleeding due to previous cesarean delivery scar defect. J Obstet Gynaecol Res. 45: 2015- 2020, 2019
5)子宮内膜症合併不妊の取り扱い
ポイント
- 子宮内膜症合併不妊の治療法は,年齢,卵巣予備能,卵管機能,パートナーの精液所見と症状および重症度を総合的に評価して選択する
- 手術適応と生殖補助医療(ART)への移行時期を適切に判断することが重要である
①子宮内膜症合併不妊の病態と治療
- 子宮内膜症合併不妊の癒着や卵巣内膜症性囊胞による骨盤内臓器の解剖学的異常と,免疫・内分泌の異常による骨盤内環境の変化が考えられる(表9).
- 画一的な治療方針を示すことは難しいが,生殖補助医療(ART:assisted reproductive technology)を視野に入れ,治療方針を決定する.

②治療方針
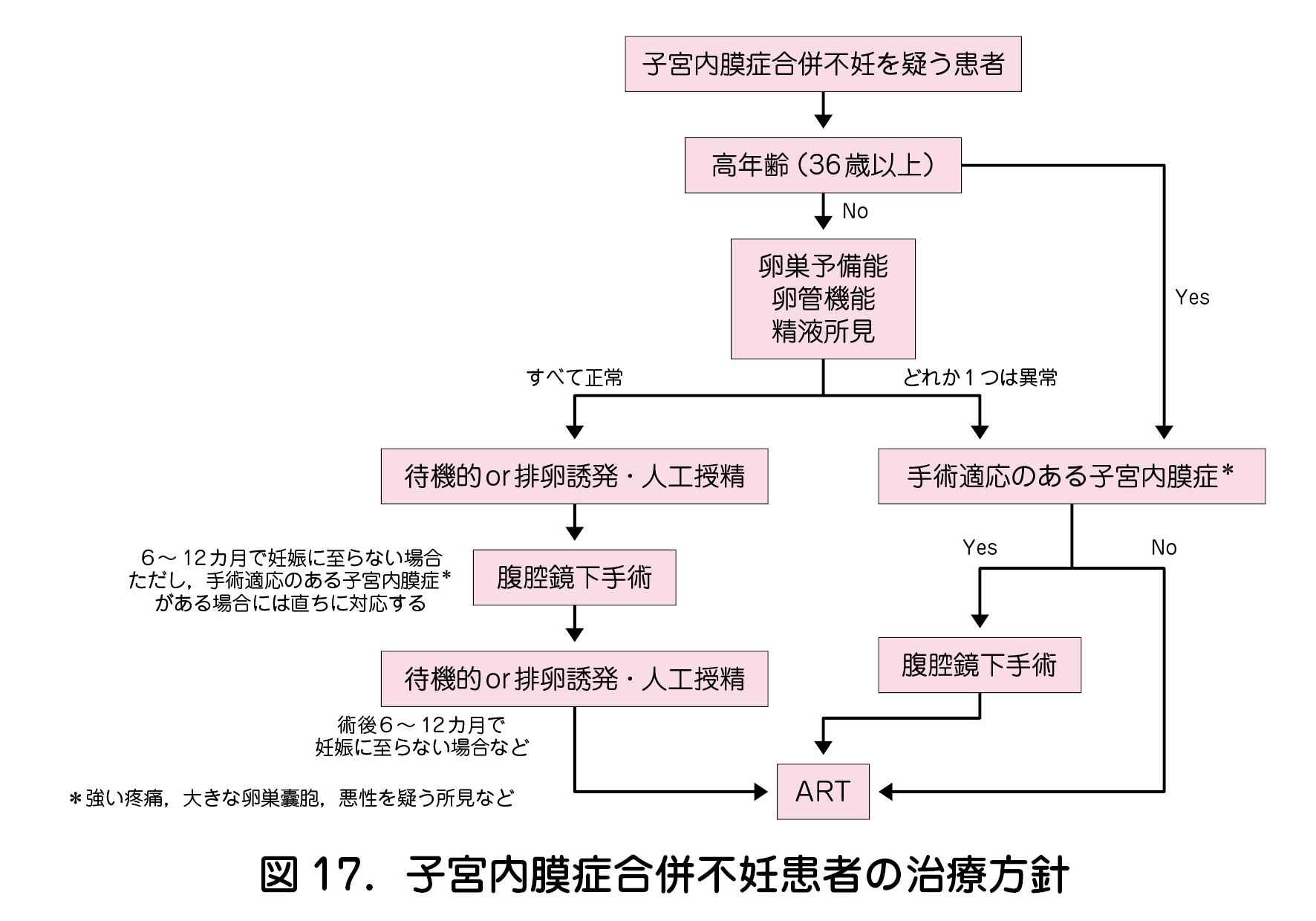
- 子宮内膜症合併不妊患者の治療方針(フローチャート)を図17に示す1).
- まずは年齢,卵巣予備能,卵管機能,パートナーの精液所見を評価する.卵巣予備能の指標には,血中抗ミュラー管ホルモン(AMH:anti-Müllerian hormone)値を用いる(ただし,AMH測定は生殖補助医療管理料算定医療機関でのみ算定される).
a.患者年齢に応じた対応
- 患者の年齢が高い(36歳以上の)場合,手術適応がない限りはARTを勧める.疼痛が強い場合や,大きな卵巣子宮内膜症性囊胞があり,破裂や感染のリスク,採卵の妨げになる場合,悪性病変の除外ができない場合などは腹腔鏡下手術を考慮する.
- 患者の年齢が若い(35歳以下)場合,卵巣予備能,卵管機能,パートナーの精液所見が正常であれば,待機的管理や一般不妊治療(排卵誘発や人工授精)を行う.12カ月を上限として妊娠が得られなければ,ARTによらない妊娠を期待して腹腔鏡下手術を考慮する.術後も12カ月を上限として待機的管理や一般不妊治療を行い,妊娠に至らなければARTを勧める.
b.卵巣因子への対応
- 卵巣予備能の低下を認める場合,手術療法が必要でなければARTを優先する.両側の囊胞摘出は,著しい卵巣予備能低下が危惧されるため,妊孕性向上目的での手術は望ましくない2,3).
- 卵巣子宮内膜症性囊胞を有する患者では,卵巣予備能が既に低下していることも多いため,ARTを開始する時期を逸しない配慮が必要である.
c.卵管因子への対応
- 卵管機能に異常を認め,自然妊娠が望めない場合には,ARTへの移行を勧める.卵管の高度癒着を伴うような中等度/重度の子宮内膜症に対して腹腔鏡下手術を行っても,妊孕性を向上させる効果は大きくない4,5).
d.疼痛増悪への対応
- 待機的管理や一般不妊治療を漫然と続けると,子宮内膜症が進行し,排卵誘発により病状が悪化する可能性もある.疼痛の増悪を認めた場合は,GnRH アゴニスト・アンタゴニスト,プロゲスチン,LEP(low-dose estrogen progestin)などのホルモン療法を一定期間投与するのが効果的であるが,一般不妊治療前のホルモン治療が妊娠成績の向上に有用であるとするエビデンスはない.ART施行前では有用であるとするエビデンスが散見されるが,至適投与期間や薬剤については,さらなる研究結果が待たれる.
文献
- 1)日本産科婦人科学会編.子宮内膜症取扱い規約 第2 部 診療編 第3 版.東京,金原出版.23-27,2021
- 2)Taniguchi F, et al. Analysis of pregnancy outcome and decline of anti-Mullerian hormone after laparoscopic cystectomy for ovarian endometriosis. J Obstet Gynaecol Res. 42: 1534-1540, 2016
- 3)Hirokawa W, et al: The post-operative decline in serum anti-Mullerian hormone correlates with the bilaterality and severity of endometriosis. Hum Reprod. 26: 904-910, 2011
- 4)Practice Committee of the American Society for Reproductive Medicine. Endometriosis and infertility: a committee opinion. Fertil Steril. 98: 591-598, 2012
- 5)Dunselman GA, et al. ESHRE guideline: management of women with endometriosis. Hum Reprod. 29(3): 400-412, 2014
6)子宮筋腫合併不妊の取り扱い
ポイント
- 子宮筋腫は生殖年齢女性で高頻度に認められ,妊娠に対する負の影響が問題となる.
- 子宮粘膜下筋腫に対する子宮鏡手術は妊娠率を改善するため積極的に行う.
- ほかに不妊原因が明らかでなく,子宮腔の変形を来している子宮筋層内筋腫は手術を検討する.
①子宮筋腫による不妊症発症機序
- 子宮筋腫による不妊症の機序として以下が挙げられる1~8).
- a.子宮腔の変形
- b.卵管閉塞・狭窄
- c.子宮の機能的変化としての子宮収縮増加や子宮内膜血流障害
- d.子宮筋腫から分泌される生化学因子による子宮内膜へ負の作用
- 子宮筋腫の位置とサイズが妊孕能に影響を与える要素である.
- 子宮粘膜下筋腫は特に妊娠率を低下させる9,10).
②手術療法の適応
- 子宮筋腫合併不妊に対する子宮筋腫核出術は,子宮筋腫の位置と子宮腔の変形を念頭に置いて手術方針を立てる11).
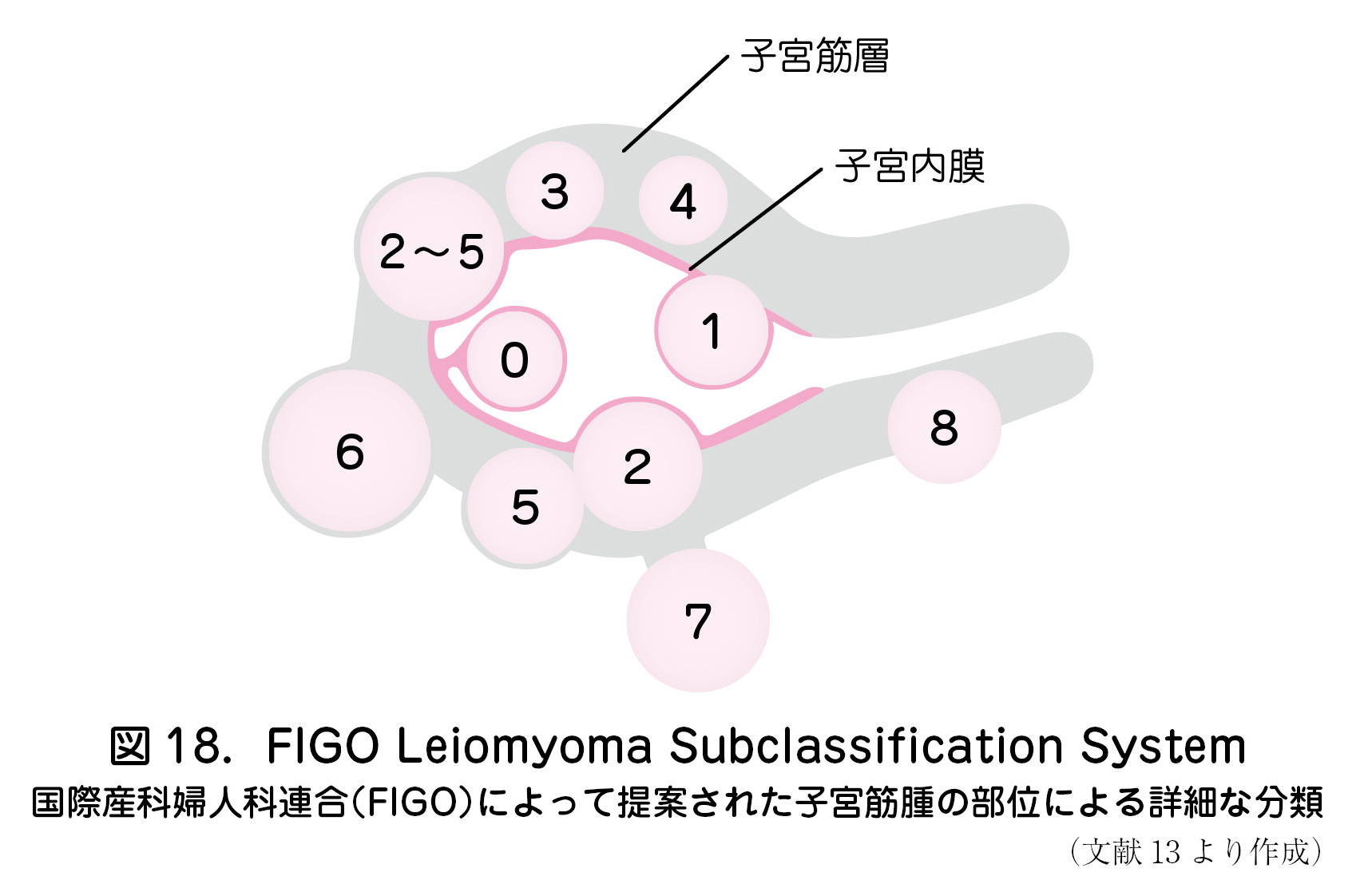
- 子宮粘膜下筋腫(FIGO Leiomyoma Subclassification System;0,1,2)に対する子宮鏡手術は,自然妊娠またはARTにおける妊娠率を改善するため積極的に行う(図18).
- 子宮鏡手術の条件は一般的に子宮筋腫直径が30~40mm以下で子宮腔への突出率が50%以上を目安とする.
- 子宮鏡手術前の子宮鏡検査が推奨される12).子宮鏡で摘出困難と予想される場合は,腹腔鏡,腹腔鏡補助または開腹による子宮筋腫核出術を検討する.
- 長径が5~6㎝を超える子宮筋層内筋腫(FIGO Leiomyoma Subclassification System;3,4,5)またはそれ以下のサイズでも子宮腔の変形を伴う場合,子宮筋腫核出術が術後の妊娠率改善に寄与する可能性がある(図18)13).
③手術の方法
- 子宮鏡,腹腔鏡,腹腔鏡補助,開腹による子宮筋腫核出(摘出)術がある.
- 正しい剝離層で操作する.
- 切開創の数を減らし術後の癒着防止に努める.
- 卵管を避ける切開をする.
- 縫合終了後は子宮を温生理食塩水で洗浄し血塊を除去し,術後感染と癒着を防止する.
- 子宮筋腫核出術時の手技では,子宮切開を可能なら前壁側から行い,妊娠に重要な子宮後壁に癒着を形成しないように注意を払う14).
- 開腹による子宮筋腫核出術後の癒着は前壁側で55%,後壁側では94%の確率で発生するとされ,生殖において重要な問題である15).
④子宮筋腫合併妊娠の予後と妊娠分娩管理
- 胎位異常,前置胎盤,常位胎盤早期剝離,羊水量の異常,早産の頻度が増加する16~21).
- 妊娠中に子宮筋腫部位に一致した一過性疼痛を認めることがある.
- 分娩時の陣痛異常,異常出血,分娩停止に注意する.
- 子宮筋腫は常位胎盤早期剝離剝離のリスクを2倍以上増加させる(OR2.29,95%CI1.62-2.96)21).特に子宮粘膜下,胎盤後方,体積200mL以上(直径7~8㎝に相当)の子宮筋腫は,常位胎盤早期剝離剝離に注意する.
⑤不妊治療中に増大する場合の対応
子宮腔の変形を来す子宮筋腫は妊孕能に影響を与え,手術的治療によってその障害を軽減することができる11).不妊症は多因子性をもつことが多く,子宮筋腫に対する治療を行う前に,パートナーを含めた不妊症の評価をすることが推奨される22).
文献
- 1)Cook H, et al. The impact of uterine leiomyomas on reproductive outcomes. Minerva Ginecol. 2010: 62(3), 225-236
- 2)Somigliana E, et al. Fibroids and female reproduction: a critical analysis of the evidence. Hum Reprod Update. 2007: 13(5),465-476
- 3)Bulun SE. Uterine fibroids. N Engl J Med. 2013: 369(14),1344-1355
- 4)Khaund A, Lumsden MA. Impact of fibroids on reproductive function. Best Pract Res Clin Obstet Gynaecol. 2008: 22(4),749-760
- 5)Pritts EA, Parker WH, Olive DL. Fibroids and infertility: an updated systematic review of the evidence. Fertil Steril. 2009: 91(4),1215-1223
- 6)Rackow BW, Taylor HS. Submucosal uterine leiomyomas have a global effect on molecular determinants of endometrial receptivity. Fertil Steril. 2010: 93(6),2027-2034
- 7)Unlu C, et al. Expression of Endometrial Receptivity Genes Increase After Myomectomy of Intramural Leiomyomas not Distorting the Endometrial Cavity. Reprod Sci. 2016: 23(1),31-41
- 8)Navarro A, et al. Understanding the Impact of Uterine Fibroids on Human Endometrium Function. Front Cell Dev Biol. 2021: 9,633180
- 9)Kroon B, et al, Australasian CCEPoTeg. Fibroids in infertility–consensus statement from ACCEPT (Australasian CREI Consensus Expert Panel on Trial evidence). Aust N Z J Obstet Gynaecol. 2011: 51(4), 289-295
- 10)Dokuzeylül et al. Surgical removal of FIGO type 0 and 1 fibroids ameliorates the expression of endometrial proinflammatory transcription factors and receptivity modulators. Fertil Steril. 2023: 119(3),504-513
- 11)Practice Committee of the American Society for Reproductive Medicine. Removal of myomas in asymptomatic patients to improve fertility and/or reduce miscarriage rate: a guideline. Fertil Steril. 2017: 108(3),416-425 12)日本産科婦人科学会,日本産婦人科医会. 産婦人科診療ガイドライン婦人科外来編2023.2023
- 13)Munro MG, et al. FIGO classification system(PALM-COEIN)for causes of abnormal uterine bleeding in nongravid women of reproductive age. Int J Gynaecol Obstet. 2011: 113(1),3-13
- 14)Carranza-Mamane B, et al. The management of uterine fibroids in women with otherwise unexplained infertility. J Obstet Gynaecol Can. 2015: 37(3),277-285
- 15)Tulandi T, Murray C, Guralnick M. Adhesion formation and reproductive outcome after myomectomy and second-look laparoscopy. Obstet Gynecol. 1993: 82(2),213-215
- 16)Wallach EE, Vu KK. Myomata uteri and infertility. Obstet Gynecol Clin North Am. 1995: 22(4),791-799
- 17)Klatsky PC, et al. Fibroids and reproductive outcomes: a systematic literature review from conception to delivery. Am J Obstet Gynecol. 2008: 198(4),357-366
- 18)Lam SJ, Best S, Kumar S. The impact of fibroid characteristics on pregnancy outcome. Am J Obstet Gynecol. 2014: 211(4),395 e1-5
- 19)Lev-Toaff AS, et al. Leiomyomas in pregnancy: sonographic study. Radiology. 1987: 164(2),375-380
- 20)Shavell VI, et al. Adverse obstetric outcomes associated with sonographically identified large uterine fibroids. Fertil Steril. 2012: 97(1),107-110
- 21)Jenabi E, Ebrahimzadeh Zagami S. The association between uterine leiomyoma and placenta abruption: A meta-analysis. J Matern Fetal Neonatal Med. 2017: 30(22),2742-2746
- 22)Infertility Workup for the Women’s Health Specialist: ACOG Committee Opinion, Number 781. Obstet Gynecol. 2019: 133(6),e377-e384
7)子宮腺筋症合併不妊症への対応
ポイント
- 経腟超音波断層法およびMRIの所見により子宮腺筋症の病態と重症度を把握し,子宮内膜症や子宮筋腫の合併の有無を確認する(表10).
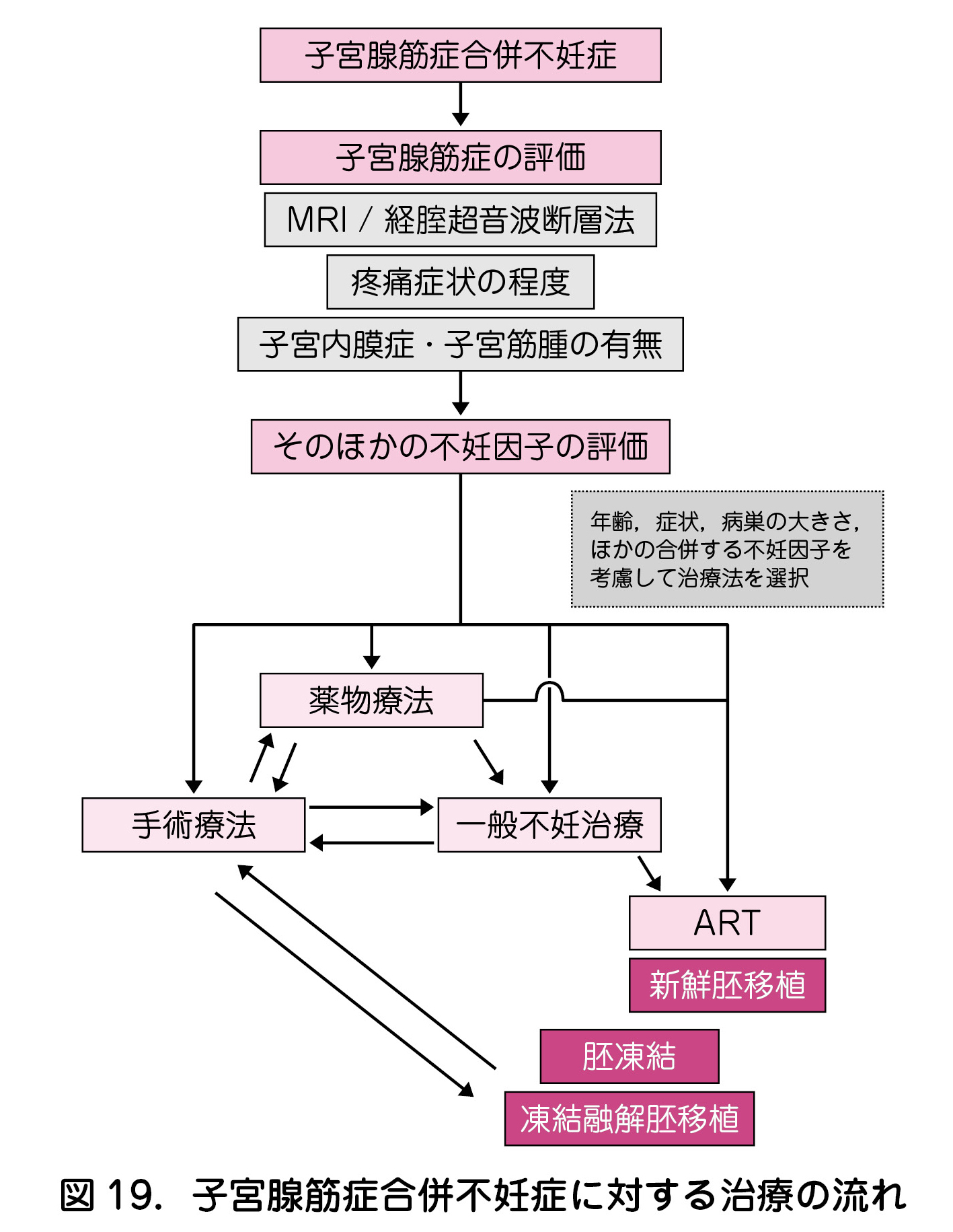
- 子宮腺筋症に対する不妊治療では,年齢,症状,病巣の大きさ,ほかの合併する不妊因子を考慮して治療法を選択する(図19).
- 手術療法,内分泌療法および生殖補助医療(ART)による複合的な不妊治療が選択されるため,年齢を考慮した早めの専門施設へのコンサルトが望ましい.
- 子宮腺筋症合併妊娠はハイリスク妊娠であり,高次周産期センター施設へ紹介する.
①子宮腺筋症と不妊症
a.子宮腺筋症の病態
子宮腺筋症は,子宮筋層内に子宮内膜類似組織が周囲に線維性組織を伴いながら増殖・進展して子宮腫大を呈し,月経困難症,慢性骨盤痛,不正性器出血,不妊症などの原因となる.子宮内膜症の類縁疾患であり,以前は内性子宮内膜症と呼ばれていたこともあるが,独立した疾患概念である.
病態仮説として3つの成因が挙げられている.
- 子宮内腔側から直接筋層に浸潤していくもので,分娩や流産手術などを起点とした子宮内膜基底層の損傷が原因と考えられており,経妊婦に多い.
- 子宮漿膜側から浸潤して病巣を形成するもので,経卵管的な月経血の逆流が関連すると考えられており,子宮内膜症との合併が多い.
- 子宮筋層内に遺残したミュラー管組織が化生して病巣を形成したもので,比較的若年で認められる囊胞性腺筋腫の原因と推測されている.
これら異なる病態が混在して存在することもある.
子宮腺筋症が妊孕性に与える影響として,子宮内膜直下の筋層の蠕動障害や子宮内膜の発育不全あるいは子宮内膜局所の慢性炎症による着床障害,精子の輸送障害がある一方で,合併することが多い子宮内膜症や子宮筋腫の影響も考慮する必要がある.また,妊娠成立後も周産期合併症が多いことが指摘されている.子宮腺筋症の病巣の大きさや占拠形態の多寡により妊孕性に与える影響も異なるため,病態の違いを念頭においたアプローチが重要となる.びまん性に子宮が腫大した例や卵巣予備能が低下した例では治療抵抗性である.
b.子宮腺筋症の診断
子宮腺筋症の確定診断は病理学的になされるが,不妊症女性における子宮腺筋症の診断には画像検査が用いられる(図19).
経腟超音波断層法では,子宮腫大に伴う内膜直下のエコー輝度の増大と低エコー櫛あるいは簾状の線条(linear striations),不均一な筋層と小囊胞,ドプラによる筋層血流の増大などが認められる.
MRIでは,限局性あるいはびまん性の病変が,子宮腫大とJZ(junctional zone)の拡張(>12mm),子宮筋層中の境界不明瞭な低信号領域の増大とその中のT2高信号スポットとして捉えられる(表10).
腺筋症病巣の形態や占拠部位,占拠範囲から限局性,びまん性,囊胞性腺筋腫,内側(intrinsic)型,外側(extrinsic)型,混合型など様々な呼称で分類されるが,統一されたものはない.

②子宮腺筋症に対する不妊治療
年齢,症状,病巣の大きさ,ほかの合併する不妊因子を考慮して治療法を選択する(図19).
a.薬物療法
子宮腺筋症はエストロゲン依存性疾患であるため,エストロゲン産生に拮抗して排卵を抑制する内分泌療法が用いられる.
子宮腺筋症(および合併する子宮内膜症や子宮筋腫)に対して,プロゲスチンやGnRH アゴニストあるいはアンタゴニスト製剤が適用される.
内分泌療法の妊娠率改善効果は必ずしも明らかでなく,妊娠可能な時期が先延ばしされるため,挙児希望例への薬物療法の適用には留意が必要である.
症状が強く子宮腫大が著明な例では,GnRHアナログ製剤を用いて一定期間薬物療法を行い,腺筋症病巣のサイズや活動性を抑制した上で妊娠を試みる.
b.手術療法
開腹あるいは腹腔鏡下に腺筋症病巣を可及的に切除する機能温存手術が試みられているが,統一された術式はなく,温存手術を行う施設も限定的である.腺筋症病巣上の漿膜下筋層をフラップのように子宮体部から分離して病巣を露出し,コールドナイフあるいは電気メスなどの様々なパワーデバイスを用いて腺筋症病巣を掘削・摘除した上で,残しておいたフラップとなる筋層・漿膜を用いて体部を縫合形成する術式が本邦で多く行われている.こうした術式は,一般に限局性の腺筋症に適用されるが,びまん性の腺筋症にも適用する術式も工夫されている.高周波凝固切開装置を用いた術式が先進医療として施行されてきたが,2023年3月で先進医療としての取り扱いが中止になっている.
手術の妊娠率改善効果は必ずしも明らかでないが,術後の妊娠例の報告は少なくない.一方で,本疾患の特徴から完全切除は困難なことが多く,術後にホルモン療法を行わない不妊症例においては,再発にも留意する必要がある.
妊娠した場合には,子宮破裂や癒着胎盤のリスクが上昇することが指摘されている.術後の子宮筋層の虚血性変化の回復を画像検査などで確認した上で妊娠許可することが望ましい.
c.生殖補助医療(ART)
ARTは子宮腺筋症に対する直接的な治療ではないが,子宮腺筋症合併不妊症に対して有効なアプローチである.凍結融解胚移植は子宮腺筋症に対する内分泌薬物療法や手術療法と併用しつつ施行可能である.
子宮腺筋症合併不妊症では高年齢の不妊女性が多く,手術療法で必要となる術前後での避妊期間を考慮すると,ARTで採卵および胚凍結を先行させた上で手術療法を行うことで,待機期間による妊孕性低下を避けることができる.一方,子宮腺筋症の自他覚症状には内分泌療法が有効であり,GnRHアナログ療法は病巣縮小効果をもつ.GnRH アゴニストあるいはアンタゴニストを一定期間使用して腺筋症病巣を縮小させた上で,そのままホルモン補充療法下に凍結融解胚移植を行う.胚移植時には少なからず病巣の活動性は再燃するため,それらの影響を考慮する必要がある.
子宮腺筋症合併不妊症では,手術療法,内分泌療法およびARTを併用した複合的な不妊治療が選択されるため,一般不妊治療で妊娠しない場合は早めに専門施設にコンサルトした方がよい.
③妊娠後の周産期管理について
子宮腺筋症合併妊娠はハイリスク妊娠である.
流早産,前期破水,頸管無力症,胎盤位置異常,妊娠高血圧症候群,胎児発育不全などのリスクが上昇する.
腺筋症による子宮内炎症,線維化による子宮筋の進展不良,子宮内膜の脱落膜化不全に起因する胎盤形成異常などが関与し,機能温存手術後の例では子宮破裂や癒着胎盤などの重篤な周産期合併症のリスクも考慮する必要がある.また,母体の高年齢やART妊娠の増加も腺筋症合併妊娠における周産期リスクの上昇に相乗的に関与する.血液凝固異常との関連の報告もあり,出血やDICの増加のリスクもある.
子宮腺筋症合併妊娠は高次周産期センター施設での妊娠管理,早期の入院,温存手術施行例では選択的帝王切開を考慮する.
8)男性患者の治療
ポイント
- 男性不妊症に対するクロミフェンクエン酸塩と,男性不妊症としての勃起不全に対するホスホジエステラーゼ阻害薬が保険適用となった.
- 男性不妊症としての逆行性射精に対しては,アモキサピンが保険診療として処方できる.
- 精巣内精子採取術(TESE,micro-TESE)が保険適用となり,手術適応を判断するY染色体微小欠失検査も保険適用となった.
①はじめに
今日の日本の最も深刻な社会問題の1つとして少子高齢化が存在するのは疑いようのない事実である.今日まで日本人年間出生数は減少の一途を辿っており第1次ベビーブーム期には約270万人,第2次ベビーブーム期には約210万人であったが,2016年には100万人を割り込む97万6,978人,2021年には過去最少の81万1,604人であり,さらに2022年は79万9,728人と過去最少を更新した.上記の状況に鑑み2022年4月1日より人工授精,生殖補助医療(ART)を含む不妊治療が保険適用された.
②男性不妊症の治療
a.薬物療法
ア 非内分泌療法
男性不妊症の原因の約8割が造精機能障害であり,その半数が特発性造精機能障害である.特発性造精機能障害に対して確立された薬物治療はないものの,経験的に漢方製剤,ビタミン剤,サプリを含むそのほかの製剤がこれまで使用されてきており,その有効率はそれぞれ23.7%,18.0%,41.3%と報告されている.精子形成に要する期間は42~76日といわれており,それを考慮して3カ月程度投与することが一般的である.ビタミン類・サプリメントとしてビタミンB12,ビタミンE,ビタミンC,コエンザイムQ10,L-カルニチン,アスタキサンチン,亜鉛,マカなど,漢方製剤としては補中益気湯,八味地黄丸,牛車腎気丸などが投与されているが男性不妊症の病名で保険適用となっているビタミン剤・サプリメント・漢方製剤は今のところはない.
イ 内分泌療法
精巣にかかわるホルモン分泌は,下垂体から分泌される黄体形成ホルモン(LH)がライディヒ細胞に働きテストステロンを分泌させ,卵胞刺激ホルモン(FSH)がセルトリ細胞に働き造精機能にかかわっている.内分泌療法とは上記のLH,FSHに関連し,造精機能を高める治療法のことである.ここでは保険診療として認められている治療法をメインに解説し,自費診療で行われている治療法についても簡潔に述べる.
クロミフェンクエン酸塩(保険診療として処方可能)
2022年4月より不妊治療の保険適用拡充に伴い,クロミフェンは男性不妊症の保険診療で使用できることとなった.選択的エストロゲン受容体調整薬であるクロミフェンは視床下部で拮抗的に結合し,エストロゲンによるネガティブフィードバックを阻害し,視床下部からの性腺刺激ホルモン放出ホルモン(GnRH)分泌が亢進し,下垂体からのLHおよびFSH分泌が促進され,造精機能を刺激する.具体的にはクロミフェン50mgを隔日投与または25mgを連日投与する.2019年にSurboneらは血清テストステロン値が低く,ゴナドトロピン値が高値ではない症例にクロミフェンが有効であるとして,治療前血清テストステロン値低値の18例において,クロミフェン50mg隔日投与3カ月にて精子濃度は中央値700万/mLから1,750万/mLに有意に改善したと報告している1).
HCG/r-hFSH療法(保険診療または自費診療)
低ゴナドトロピン性性腺機能低下症(MHH:male hypogonadotropic hypogonadism)に対して保険診療として用いられる治療法である.MHHは男性不妊症外来においてLHおよびFSHが基準値以下の無精子症として診断され,ヒト絨毛性ゴナドトロピン(HCG)製剤3,000~5,000単位を週2回,組み換えヒト卵胞刺激ホルモン(r-hFSH)製剤75~150単位を週3回で開始し,LHおよびFSHを補充することで精子出現が期待され,自然妊娠する場合もある.しかしながら,男性不妊症患者のうちMHHは約1%程度とされている.
自費診療としては,非閉塞性無精子症(NOA:non-obstructive azoospermia)に対して顕微鏡下精巣内精子採取術(micro-TESE:microscopic testicular sperm extraction)を行い,精子が採取できなかった場合にHCGやr-hFSHを用いた内分泌療法を行った上で,2回目のmicro-TESEを行い,精子採取が可能であったと報告されている.また,低テストステロン血症を伴うNOAに対してHCGによって正常化させ,その後にmicro-TESEを行い精子採取率が改善したという報告もある.しかし,確立された方法ではないので,実際に行う際には十分なインフォームドコンセントが必要である.
アロマターゼ阻害薬(自費診療)
アロマターゼ阻害薬はテストステロンからエストラジオールに変換する酵素であるアロマターゼを阻害する結果,テストステロンの上昇とエストラジオール低下をもたらす.
ウ 性機能障害治療
男性不妊症の原因について1997年および2015年に大規模な調査が行われた.性機能障害が男性不妊症の原因に占める割合は1997年に3.3%であったが,2015年には13.3%と大幅に増加しており,今日では障害の診断および治療は重要な位置づけとなっている(13~14頁参照).ここでは保険診療可能な2つの薬剤について述べる.
ホスホジエストラーゼ(PDE5)阻害薬(保険診療として処方可能)
2022年4月より勃起障害を伴う男性不妊症に対してPDE5阻害薬が保険適用となった.しかしながら制限なく処方できるわけではなく,純粋に不妊症診療として使用されるべく保険診療として処方する上で縛りが設けられている.今回,保険給付の対象となるのは先発品であるバイアグラ®25mg錠,50mg錠,ODフィルム25mg,50mg並びにシアリス®5mg,10mg,20mgに限定されている.
逆向性射精に対するアモキサピン(保険診療として処方可能)
逆向性射精は,射精感を感じるが精液が射出されない状態を指す.オルガズムを感じた後の検尿で,精子が10~15細胞/強拡大視野以上認められた場合に診断される.アモキサピン1日量25~50mgを1日1回夕食後あるいは眠前に連日服用する.効果不十分の場合は1日量75mgまで増量する.必要時服用では1回量25~50mgを1時間前に1回服用する.
b.外科的治療
ア 精索静脈瘤手術
男性不妊症の大きな原因の1つである造精機能障害は前述したように特発性症例が多いが,原因が同定できるなかで最も頻度が高いのが精索静脈瘤である,蝕知可能な精索静脈瘤を認める精液所見不良症例では手術により一定の妊孕能の改善が期待でき,男性不妊疾患のうち最も外科的治療の介入がなされている疾患である.精索静脈瘤手術は顕微鏡下低位結紮術が最も低侵襲で手術成績が良好な術式であり,本邦でも広く行われている.顕微鏡下低位結紮術は脈管の剝離と結紮という基本手技の繰り返しであり,顕微鏡操作に慣れれば問題なく行うことができるとされている.
イ 精路再建術
閉塞性無精子症(OA:obstructive azoospermia)の頻度は無精子症の10%前後である.診断は無精子症,精巣萎縮なし(通常は片側12mL以上),卵胞刺激ホルモン(FSH)の上昇なし(明確な基準はないが7~8mIU/L未満のことが多い),既往症の聴取,触診により精管欠損や精巣上体での硬結の蝕知および鼠径部の手術痕の有無などの評価により,閉塞原因や部位を同定できることも多い.しかしながら,上記診断基準を満たしても,約10%程度に非閉塞性無精子症が存在するため注意が必要である.精路再建術(精管-精管吻合:精管結紮術や鼠経ヘルニア術後の場合など,精管-精巣上体吻合:精巣上体炎後や原因不明の場合など)により,顕微授精などの生殖補助医療(ART)を行わなくても,タイミング法や人工授精などの一般不妊治療で妊娠が可能となる.一方で,OAにおいては精巣内精子採取術(TESE)により容易に精子採取が可能であり,TESE-ICSIがしばしば施行される.今日の晩婚化に伴う妻の年齢の上昇により,TESE-ICSIを急ぐケースが多くみられるが,OAにおいては必ず精路再建術のオプションも提示しなければならない.
ウ 外科的精子採取術
診療報酬改定に伴い,2022年4月からTESEが保険適用となった.TESEは閉塞性無精子症,非閉塞性無精子症,射精障害などの患者で,ほかの方法により顕微授精に用いる精子が採取できないと医師が判断したものが対象で,単純なもの(TESE:12,400点)と顕微鏡を用いたもの(micro-TESE:24,600点)に分類される.施設基準を満たすこと,治療に当たっては治療方針について適切に検討し,該当患者カップルの同意を得ること,該当患者およびそのパートナ-が婚姻関係または出生した子について認知を行う意向があることの確認に加えて,女性の年齢が該当生殖補助医療の開始日において43歳未満であることが必要である.また,施設基準を満たせば,精巣内精子採取術の適応の判断を目的に,Y染色体微小欠失検査が保険適用(3,770点)となった.
精巣内精子採取術(TESE)
閉塞性無精子症で精路再建を患者が希望しない場合や,先天性精管欠損症などで精路再建を行うことが困難な場合や射精障害などの患者でほかの方法により精子採取が困難な症例に対しては手術用顕微鏡を使用しないc-TESE(conventional-TESE)が適応になる.局所麻酔下での日帰り手術が可能であり,陰囊皮膚を切開し,精巣白膜を露出させ5mmほど切開し,精巣内の精細管を鑷子で採取する.採取した精細管内の精子を確認し,精子が確認されればこれをICSIに使用する.術前に閉塞性無精子症と予測された場合でも,術中所見によっては手術用顕微鏡を使用するいわゆるmicro-TESEへ移行する可能性があることを十分に説明しておく.
顕微鏡下精巣内精子採取術(micro-TESE)
非閉塞性無精子症に対するTESEは手術用顕微鏡を使用するmicro-TESEが行われる.手術適応を判断するために術前にY染色体微小欠失検査を行うべきであり2022年4月より保険適用となっている.Y染色体の微小欠失検査でAZF(Azoospermiafactor)領域のAZF a,AZF b,AZF b+c領域の欠失では精子回収は期待できない2).局所麻酔でも手術可能であるが,全身麻酔,脊椎麻酔で行われることもある.陰囊縫線に沿って約2~3㎝程度の縦切開をおき,陰囊の内容を脱転する.精巣白膜を切開し,手術用顕微鏡で精巣内容をよく観察する.非閉塞性無精子症で精子回収が可能な場合,精巣内の精細管は不均一であり,精子が存在する可能性が高い.太く白濁した精細管を採取し,採取した精細管を細切し培養液中の精子の有無を確認する.精子が確認されれば,これをICSIに使用する.文献によって差が大きいが,micro-TESEにおける精子回収率はおよそ30~50%程度という報告が多い3).
文献
- 1)Surbone A, Vaucher L, Primi MP, Leyvraz C, Pitteloud N, Ballabeni P, Mathevet P, Vulliemoz N. Clomiphene citrate effect on testosterone level and semen parameters in 18 infertile men with low testosterone level and normal/low gonadotropines level. Eur J Obstet Gynecol Reprod Biol. 238: 104-109, 2019
- 2)Simoni M, Bakker E, Krausz C. EAA/EMQN best practice guidelines for molecular diagnosis of y-chromosomal microdeletions. State of the art 2004. Int J Androl. 27: 240-249, 2004
- 3)Schlegel PN. Testicular sperm extraction: microdissection improves sperm yield with minimal tissue excision. Hum Reprod. 14: 131-135, 1999
9)タイミング法
ポイント
- 排卵日は月経周期・腟分泌物の状況を参考にしつつ,経腟超音波検査による卵胞径および血中E2,LHの値から予測する.
①タイミング法を選択する背景
- 年齢に留意することは最重要である.35歳以上ではタイミング法に固執せず,早めに人工授精(AIH),ARTへのstep upを検討する.逆に35歳未満においては時間的猶予があり,受診するまでの期間にもよるが比較的タイミング法を勧める傾向にある.
- まずはタイミング法を行う前に,ご夫婦に問診し,現在の性交状況について確認する.意外にも男性側,女性側共に性交障害となっているケースは多い.原因として長年交際のため今は性交がないということも少なくない.また夜勤や転勤,出張などの仕事上の都合により実質的に性交が行えないこともある.社会的背景にも留意しなければならない(13~14頁参照).
- 男性側の性交障害は勃起障害(ED:erectile dysfunction)がほとんどである.「タイミングED」(指定された日に性行為をすることに対して,義務感やプレッシャーを感じることによるED)のみならず,糖尿病,高血圧,喫煙などにより勃起障害に至る.積極的にホスホジエステラーゼ阻害薬やシリンジ法を選択する(通販サイトで「シリンジ法」と検索すればキットが購入できる).
- 女性側の性交障害も存在する.陰茎の挿入で疼痛を自覚する患者は少なくない.ゼリーなどの使用を勧める.
- 精液検査の所見に留意する.正常範囲(27頁「精液検査」参照)を逸脱する場合,自然妊娠は厳しいと考えてよい.積極的に男性不妊専門外来を紹介,所見によってはAIH,ARTへのstep upを促す1).
- 超音波検査で子宮筋腫,子宮腺筋症,卵巣腫瘍(子宮内膜症,成熟奇形腫など)を確認する.着床に影響を及ぼす粘膜下筋腫および内膜に近い筋腫においては手術を勧める.腺筋症や内膜症は卵巣の位置が偏位し,卵管采の癒着を生じ,Pickup障害のリスクとなる.若年でも長い不妊期間であればstep upする.
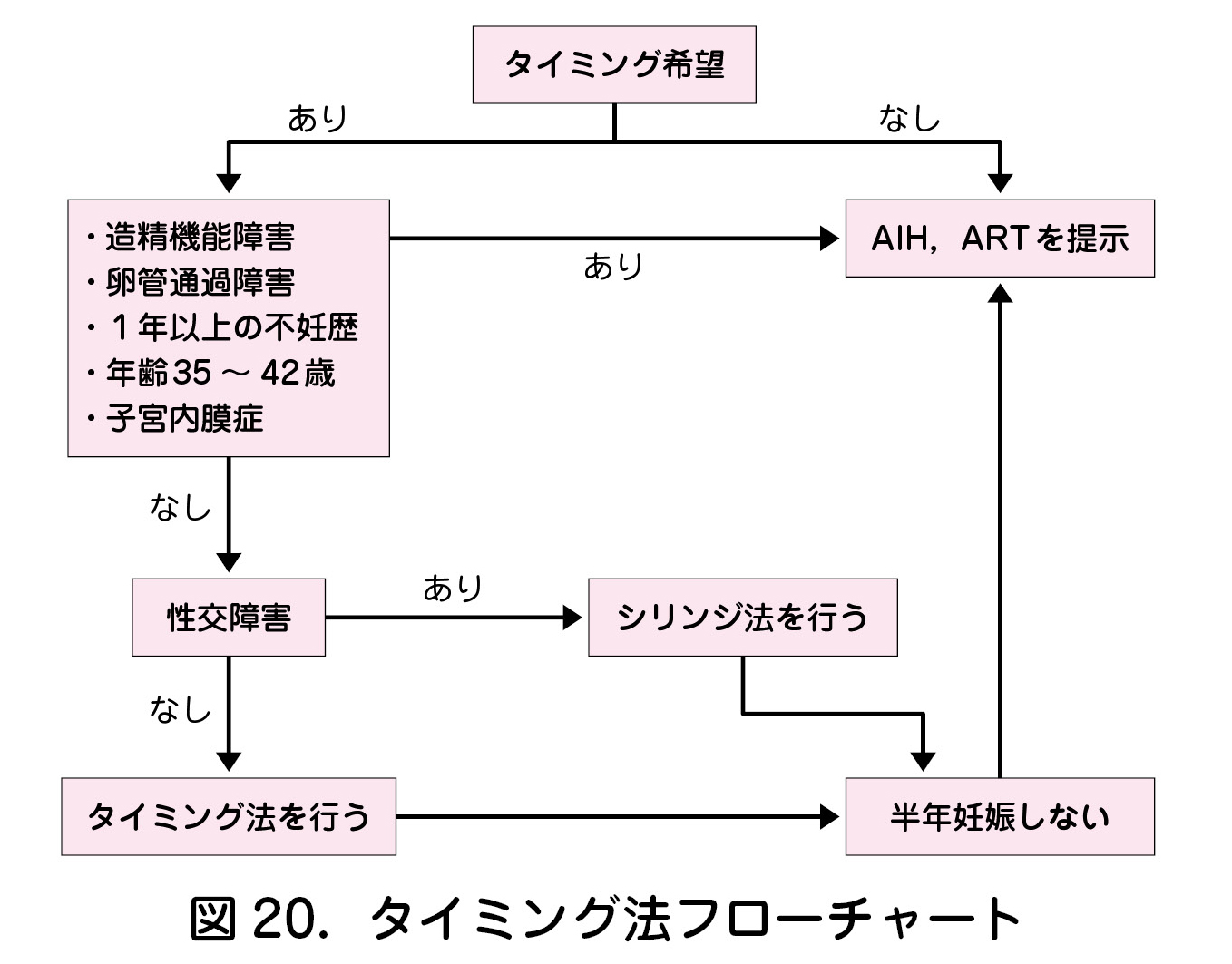
- 子宮卵管造影検査は検査後3~6カ月は妊娠率が上昇するといわれており,タイミング法を行う上で必須の検査である2)(図20).
②タイミング法における排卵誘発および検査所見
- まずは月経周期を問診にて確認する.周期が安定していないケースではタイミング法は取りづらい.周期あたり数回の通院が必要になる.
- 月経周期が安定している場合でも,卵胞が複数育つことや,保険超音波回数を増やす目的に排卵誘発剤を使用する.安定しない場合や多囊胞性卵巣症候群などで希発月経である場合は排卵誘発剤の増量を検討する.排卵誘発法については36~38頁参照.
- 超音波検査で卵胞径が約20~24mmの時に排卵する.月経周期や過去の排卵時期から次回の排卵時期を推定し,外来診察日を決める.
- 血中ホルモン値では,E2が200~400pg/mLの時に卵胞径は十分発育しており,LH上昇から約36~40時間で排卵に至る.
- 超音波検査で子宮内膜が全層白色になり卵胞が見られない場合,プロゲステロンが上昇していれば排卵後と考えられ,次周期に備える.
③カップルへの指導方法
- 時間的空間的制限によりカップルが通院できない状況もある.自宅での排卵検査薬を指示し,最も妊娠しやすい排卵1~2日前でのタイミングを促す.それでも難しい場合は一度不妊治療休止を提案し精神的,身体的苦痛をとることも大切となる.
- カップルへの心理的サポートも大切である.sexlessになっている夫婦に対しタイミング法を強いてはいけない(13~14頁参照).
文献
- 1)Van Voorhis BJ, et al. Effect of the total motile sperm count on the efficacy and cost effectiveness of intrauterine insemination and in vitro fertilization. Fertil Steril. 75: 661-668, 2001
- 2)Nugent D, et al. A randomized controlled trial of tubal flushing with lipiodol for unexplained infertility. Fertil Steril. 77: 173-175, 2002
10)人工授精
ポイント
- 排卵誘発剤を併用すると妊娠率は向上するが,多胎妊娠も増えることに注意する.
- 人工授精は排卵日に行うのが望ましいが,排卵2日前から排卵半日後までは有効と考えられる.
- 精子調整を行わない人工授精は保険適用が認められていない.
①人工授精とは
精液から運動性良好精子を回収し,排卵期の子宮腔に注入する手技である.
②人工授精の適応
「精子,精液の量的・質的異常」,「性交障害・射精障害」,「精子-頸管粘液不適合」,「機能性不妊」などが適応となる.
③人工授精と排卵誘発剤
「精子,精液の量的・質的異常」,「性交障害・射精障害」,「精子-頸管粘液不適合」を適応として人工授精を行う場合には,排卵障害がない例では自然周期から開始する.
「機能性不妊」を適応として人工授精を行う場合には,海外では排卵誘発剤を併用することが推奨されているが,本邦においては多胎防止の観点から自然周期からの開始を考慮するべきであろう.海外では人工授精の費用が高く,多胎に寛容であることなど本邦とは異なった背景がある.
④人工授精の妊娠率
人工授精の妊娠率は,体外受精と同様に年齢により異なる.治療周期当たりの30歳で10%程度,35歳で8%程度,40歳で5%程度である.排卵誘発剤を併用すると向上するが,その分多胎妊娠も増えることに注意しなくてはならない.
⑤人工授精を行うタイミング
人工授精は,排卵日に行うのが望ましいが,排卵2日前から排卵半日後までは有効と考えられる.
調整後の精子は受精可能期間が短いといわれているが,LHサージ前に人工授精を行い,人工授精直後にhCGを投与した例でも妊娠例が得られることから,排卵2日前の人工授精でも妊娠可能と考えられる.
体外受精の知見から,排卵後の卵子の受精可能期間は半日程度と考えられており,排卵後は半日以内に人工授精を行う必要がある.
体外受精で行われているように,排卵時期を合わせるためにhCGやGnRH アゴニストを使用することもあるが,尿中LHで排卵時期を合わせる場合と妊娠率は変わらない.
⑥精子調整法
以前は無調整の精液を子宮内に注入することもあったが,精液による感染のリスクや,精液中のプロスタグランディンの子宮収縮作用による疼痛などがあり,現在はほとんど行われていない.精子調整を行わない人工授精は保険適用が認められていない.精液をPBS(リン酸緩衝生理食塩水)や培養液で洗浄濃縮して子宮腔に注入する方法もあるが,精液中の細菌,白血球,不純物を精子と同時に注入することになり,望ましい手技ではない.
現在主に用いられているのは密度勾配遠心法と,MS法(migration-gravity sedimentation 法)である.両方の具体的方法について述べる.
a.連続密度勾配遠心法
パーコールなどの密度勾配担体を用いて運動良好成熟精子を選別する方法である.成熟した精子の細胞密度は1.11~1.12g/mLであるのに対し,未熟精子や死滅精子は1.09g/mLと低い.パーコールなどの密度勾配担体の密度を1.10g/mLに調整して,試験管に入れ,その上に精液を重層し,遠心沈降を行うと,成熟精子のみが担体の下に沈殿し,未熟精子や死滅精子,白血球,細菌などの担体より密度の低い物質は沈殿しない.この沈殿した成熟精子のみを回収し人工授精に用いる.
良好精子の回収率は高く,最も一般的な精子調整法であるが,精子を遠心沈降することによる精子DNAの断片化の頻度が高くなる可能性が指摘されている.
具体的な調整方法を述べる.
- 滅菌試験管にトランスファーピペットで80%パーコール液などの担体を4~6mL注入する.パーコール液以外にもいくつかの担体がready to useの形で販売されている.
- 担体の上層に,採精後20~30分間室温に置くことにより液化した精液を重層する(図21).
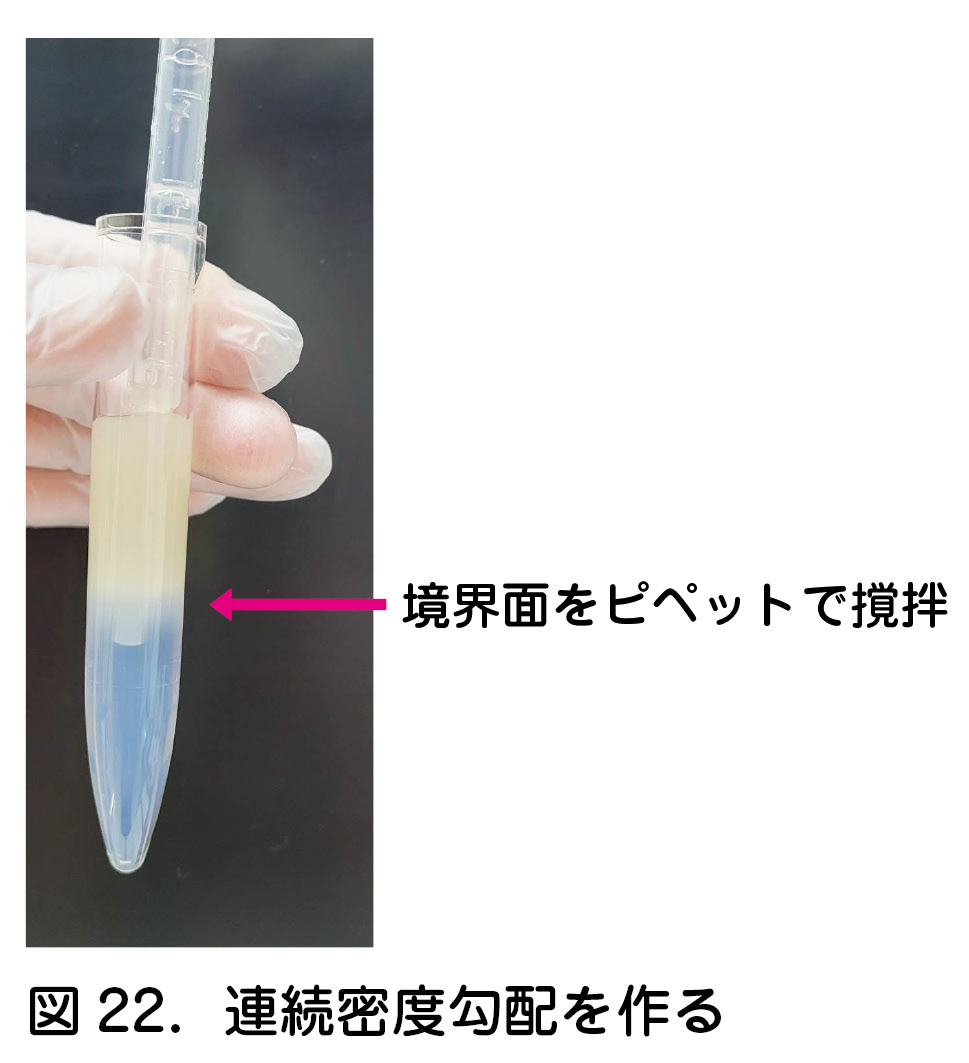
- パーコールと精液の層の間をトランスファーピペットなどでゆっくりと境界面がなくなるまで撹拌することにより連続密度勾配を作る(図22).
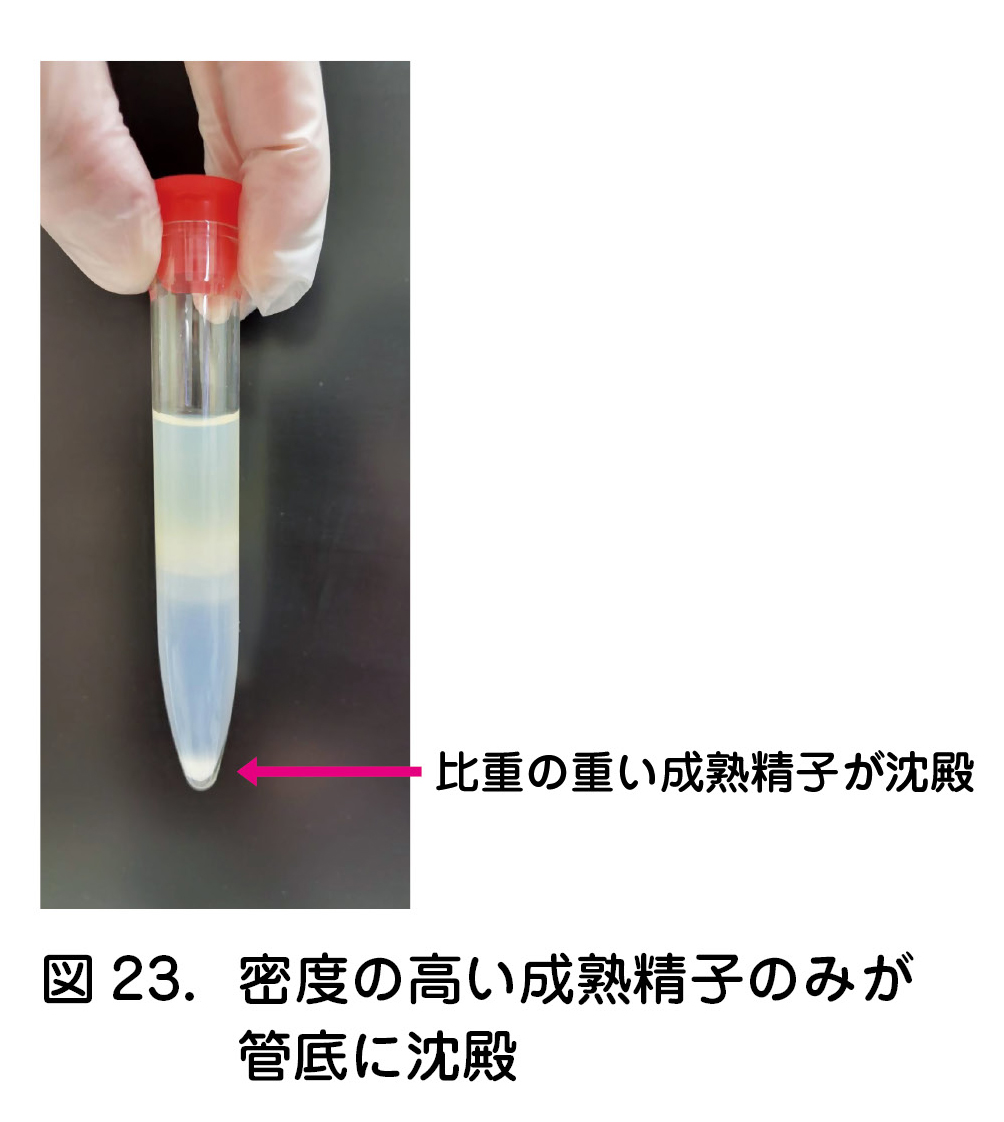
- 遠心機にこの試験管を入れ,バランスをとって600×g(通常の遠心機で2,000rpm程度)で20分間遠心する.密度の高い成熟精子のみが管底に沈殿する(図23).
- 上層の精液とパーコールをトランスファーピペットで吸引除去し,沈殿した精子と少量のパーコールのみを試験管に残し,混和し,この精子浮遊液を精子洗浄液3mLの入った Falcon 2003 試験管に移す.
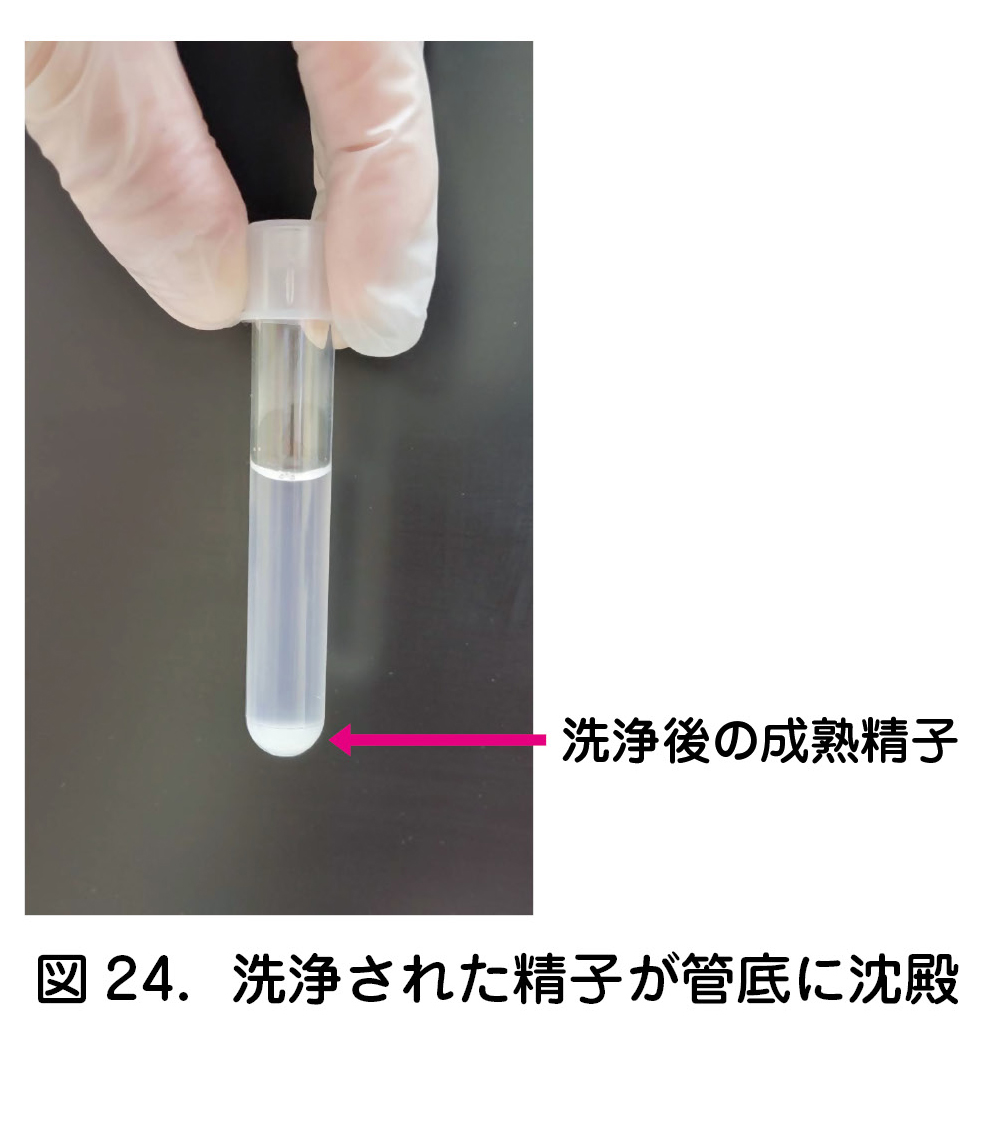
- 精子浮遊液と洗浄液をトランスファーピペットでよく混和し,200×g(通常の遠心機では1,250rpm程度)で7分間遠心すると洗浄された精子が管底に沈殿する(図24).
- 上澄みをトランスファーピペットで吸引除去し,0.5mLのみ残す.
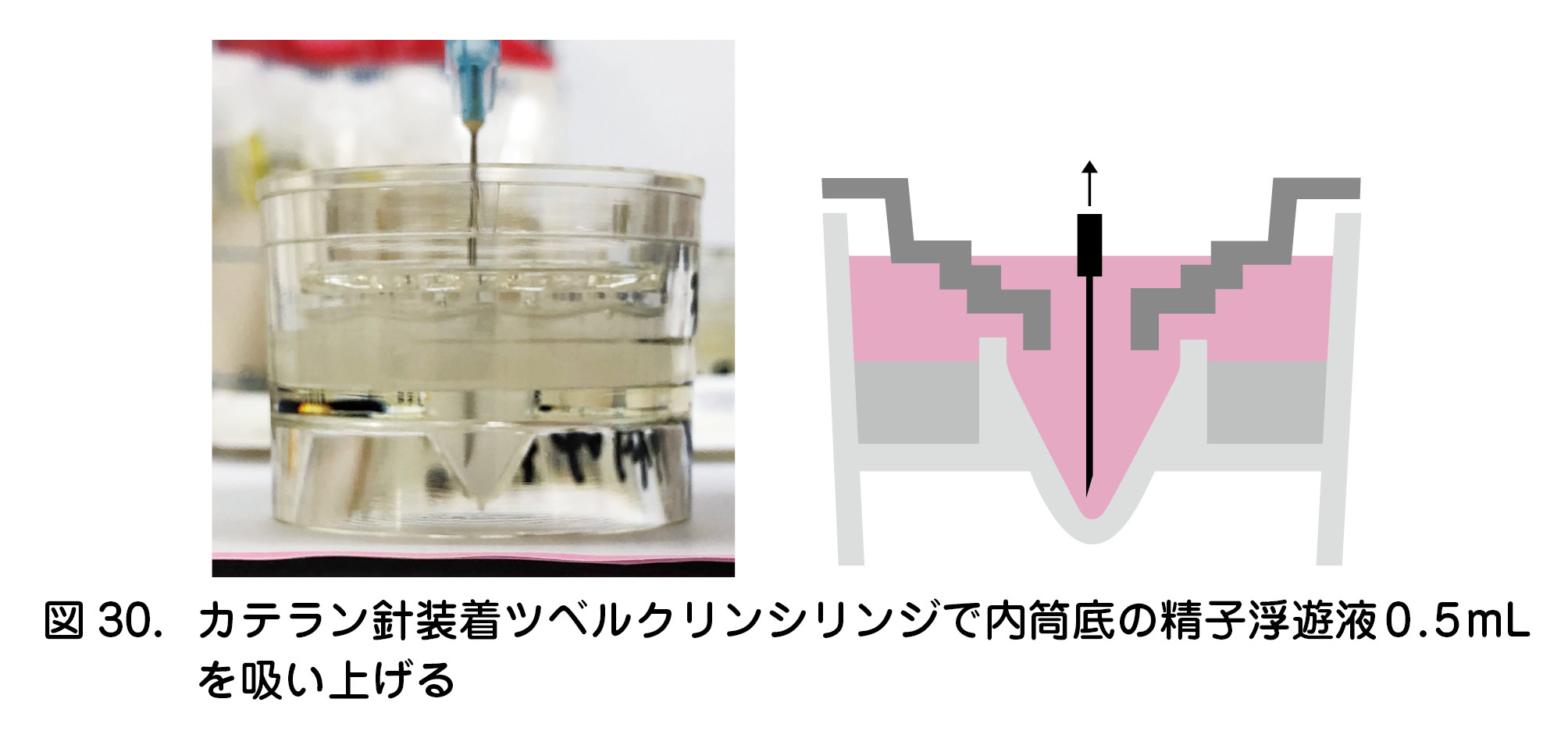
- 沈殿精子と残った精子洗浄液を混和し,22Gのカテラン針に1mLツベルクリンシリンジを装着して精子浮遊液をシリンジに吸引する.
- カテラン針を人工授精用のカテーテルに付け替え,人工授精を行う(図25).
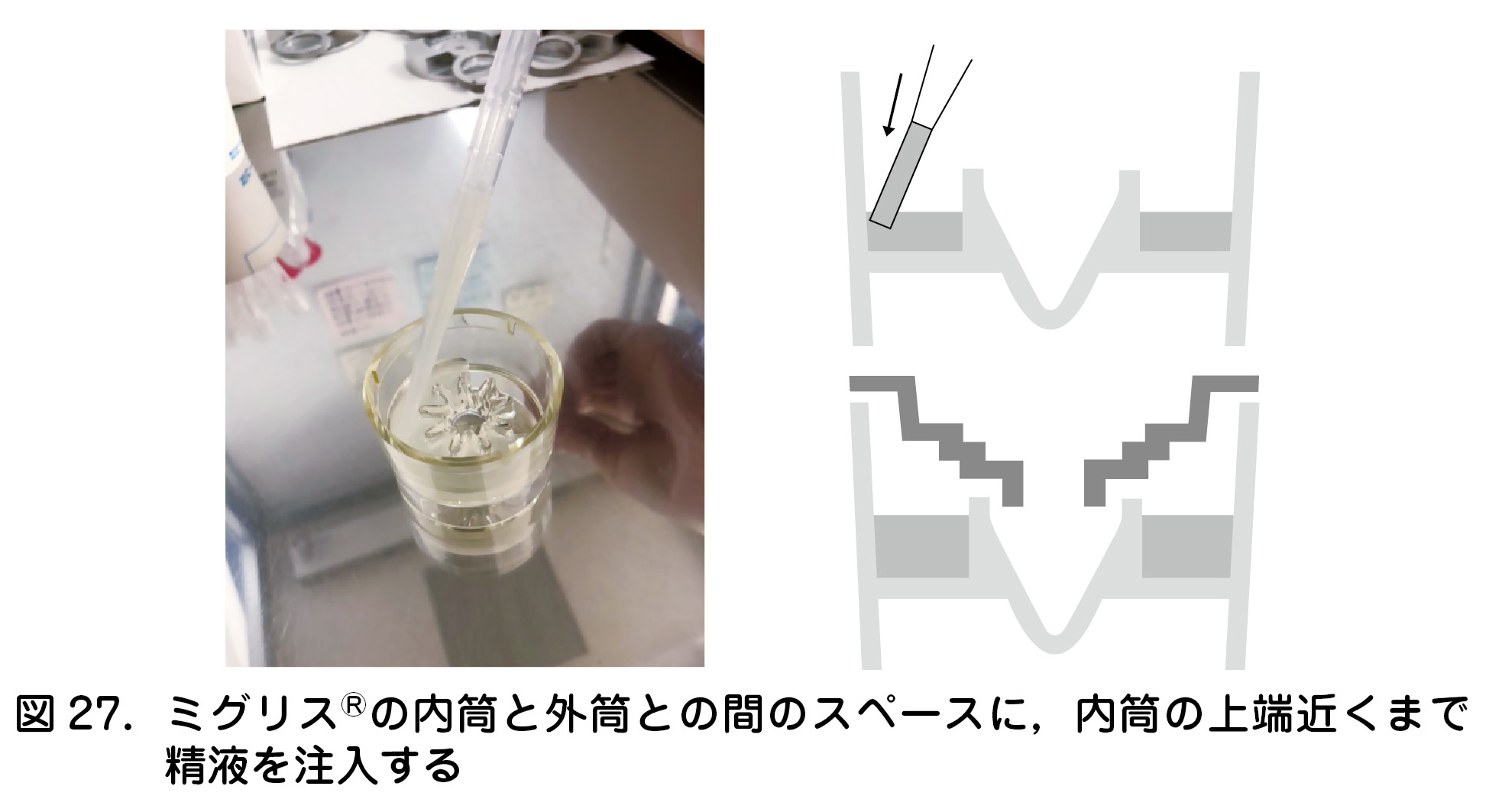
- 採精後20~30分間室温に置くことにより液化した精液を,ミグリス®の内筒と外筒との間のスペースに,内筒の上端近くまで注入する(図27).
- スペーサーを装着し,内筒の底から静かにPBS(または培養液)を注入し,内筒の上端を超えて溢れたPBSが精液の上に重層されるようにする(図28).
- 蓋をかぶせてこのまま1時間静置すると,運動精子が精液から培養液にswim-upし,内筒の下に落下して集まる(図29).
- カテラン針を装着した1mLツベルクリンシリンジで内筒の底から精子浮遊液0.5mLを吸い上げ(図30),カテラン針を人工授精用のカテーテルに付け替えて人工授精を行う(図25).
- 不妊治療に漢方薬を使用(併用)することで,妊娠しやすい体質に導くことができる.
- 東洋医学からみて不妊症は,気血水や五臓(心・肝・脾・肺・腎)のアンバランスととらえられ,五臓で特に関係が深いのは腎・肝・脾とされる.
- 女性3大漢方薬(当帰芍薬散・加味逍遙散・桂枝茯苓丸)がファーストチョイスとして役に立ち,証「タイプ」に合わせて選択される.
- 当帰芍薬散は「四肢末端型:血虚型」の冷えを改善する.血を補う当帰・川芎・芍薬,水を巡らす茯苓(ぶくりょう)・朮(じゅつ)・沢瀉(たくしゃ)を含むため,虚証(体力なし)で,貧血気味でむくみを感じるものに有効である.安胎薬であるため妊娠後も内服が可能である.
- 加味逍遥散は「体感異常型:肝鬱型」が背景にある冷えを改善する.血を補う当帰・芍薬,血を巡らす牡丹皮,水を巡らす茯苓・朮に加えて,気に効く柴胡(さいこ)・山梔子(さんしし)・薄荷(はっか)を含み,中間証(体力中程度)で気分が逍遥するものに有効である.妊娠後は基本的に休薬する.
- 桂枝茯苓丸は「上熱下寒型:瘀血型」の冷えを改善する.血を補う芍薬,血を巡らす牡丹皮・桃仁,水を巡らす茯苓,気に効く桂皮(けいひ)を含み,血を巡らす代表の漢方薬(駆瘀血薬(くおけつやく))として使用される.中間から実証(体力あり)で,冷えのぼせがあり下腹部に膨満感を訴えるものに有効である.子宮筋腫や子宮内膜症は瘀血の代表疾患なので選択するとよい.妊娠後は基本的に休薬する.
- 第一度無月経,無排卵周期症,黄体機能不全→当帰芍薬散,温経湯,桂枝茯苓丸
- 多囊胞性卵巣症候群→温経湯,芍薬甘草湯,柴苓湯
- 高プロラクチン血症・高アンドロゲン血症→芍薬甘草湯
- 子宮内膜が薄い場合(血虚)→温経湯,当帰芍薬散,加味逍遙散,当帰四逆加呉茱萸生姜湯など
- 子宮内膜が肥厚している場合(瘀血)→桂枝茯苓丸,加味逍遙散,桃核承気湯など
- 糖尿病,アルコール多飲,肥満などのメタボリックシンドローム<実証>
→大柴胡湯(だいさいことう)や防風通聖散(ぼうふうつうしょうさん) - 加齢男性性腺機能低下症(LOH症候群)<虚証>→八味地黄丸
- 胃腸が弱い場合→六君子湯,補中益気湯など
- ストレス,うつなどによる心因性→柴胡加竜骨牡蛎湯,四逆散など
- 精索静脈瘤(「瘀血」ととらえる)→桂枝茯苓丸


b.MS法
市販されているミグリス®(メニコン)というデバイスを用い,swim-upした精子を落とし穴に落として運動性良好精子を回収する方法である(図26).密度勾配遠心法やswim-up法と比べて工程は少なく遠心機も不要である.医師が診療の合間に精子調整を行うこともできる.遠心操作を加えないことから,精子DNAの断片化のリスクは低い.
具体的な調整方法を述べる.



⑦人工授精の手技
このようにして調整した精子浮遊液を人工授精用のカテーテルで子宮腔に注入する.
人工授精用のカテーテルには材質,長さ,太さ,硬さ,先端の屈曲などが異なるものが各社から販売されており,製品間での妊娠率の差はほとんどない.
クスコ式腟鏡を装着し,腟内をヂアミトールなどで消毒した後にカテーテルを外子宮口から子宮腔に挿入する.挿入困難例では必要に応じて単鈎鉗子やゾンデを使用する.カテーテルの先端が子宮底付近に達したところで,精子浮遊液を注入する.
⑧人工授精の副作用
人工授精後に軽度の出血を認めることがある.1,000例に1例程度の割合で子宮内膜炎や卵管炎,腹膜炎を起こすことがある.人工授精後に抗菌薬を1~3日間投与することが多い(保険適用外).
11)不妊治療における漢方薬
ポイント
①漢方薬を使用(併用)する理由
東洋医学における不妊症の薬物療法の歴史は古く,後漢の時代の中国の古典医学書である「金匱要略(きんきようりゃく)」に「無子」として治療処方が記されている.
妊娠は心身ともにバランスが整った健康な男女に訪れる自然生理現象であるが,昨今は,ストレスの増加や挙児希望年齢の高年化など心身のバランスの崩れが助長される環境にある.漢方薬は2種以上の生薬の組み合わせからなり,様々な作用点から男女の心身のバランスを整え,妊娠しやすい体質に導くことができる.単独使用はもちろん最先端の生殖補助医療(ART)に漢方薬(東洋医学)を併用することで,子を望む夫婦の福音につながる.
②東洋医学からみた不妊症
不妊治療において,五臓で関係が深いのは腎・肝・脾とされる.生殖機能は,男女ともに五臓のうち「腎」が関与するとされており,不妊症は腎の機能が低下した「腎虚(じんきょ)」と考えられ,「補腎剤」の八味地黄丸(はちみじおうがん)などが適応となる.高年になるほど,腎虚の要因が強くなる.若年でも睡眠・食事の異常,ストレス過剰が腎虚につながるため養生(生活習慣)も重要視される.「肝」は血を貯蔵するとともに,自律神経を介して気血を巡らす働きをもつ.ストレスで生じる「肝鬱(かんうつ)」を解消するには加味逍遙散などの「柴胡剤」が使用される.また「脾」は消化吸収の働きを持ち栄養の補充に重要な働きをする.「脾虚:胃腸虚弱」は最初に治療する必要があり「補脾剤」の六君子湯(りっくんしとう)などが選択される.
また,気血水(気:エネルギー,血:血液など,水:血漿など)のアンバランスは,気虚(エネルギー不足)・気鬱(抑うつ気分など)・気逆(いらいらやホットフラッシュなど)・血虚(栄養不足や貧血など)・瘀血(血流の滞り)・水滞(むくみなど)が挙げられ不調につながる.
女性の場合,気血水や五臓のバランスが整うと冷えが改善され,子宮卵巣への血流が保持され妊娠しやすい体質に近づくことができる.温かく緊張のない丸い腹を指標にする.妊娠を望む前から,月経異常や体調不良への早期介入や妊娠適齢期の存在を伝えていくことも大切である.
③漢方薬選択の実際
a.女性3大漢方薬を選択する
女性3大漢方薬とは当帰芍薬散(とうきしゃくやくさん)・加味逍遙散(かみしょうようさん)・桂枝茯苓丸(けいしぶくりょうがん)であり,気血水のバランスを整え,冷えを改善することができる4).女性の不調に対しては「血を補い,血を巡らす」のが基本であり,それは不妊治療においても原則となる.これが,血に作用する生薬を含む女性3大漢方薬をファーストチョイスとする理由である.
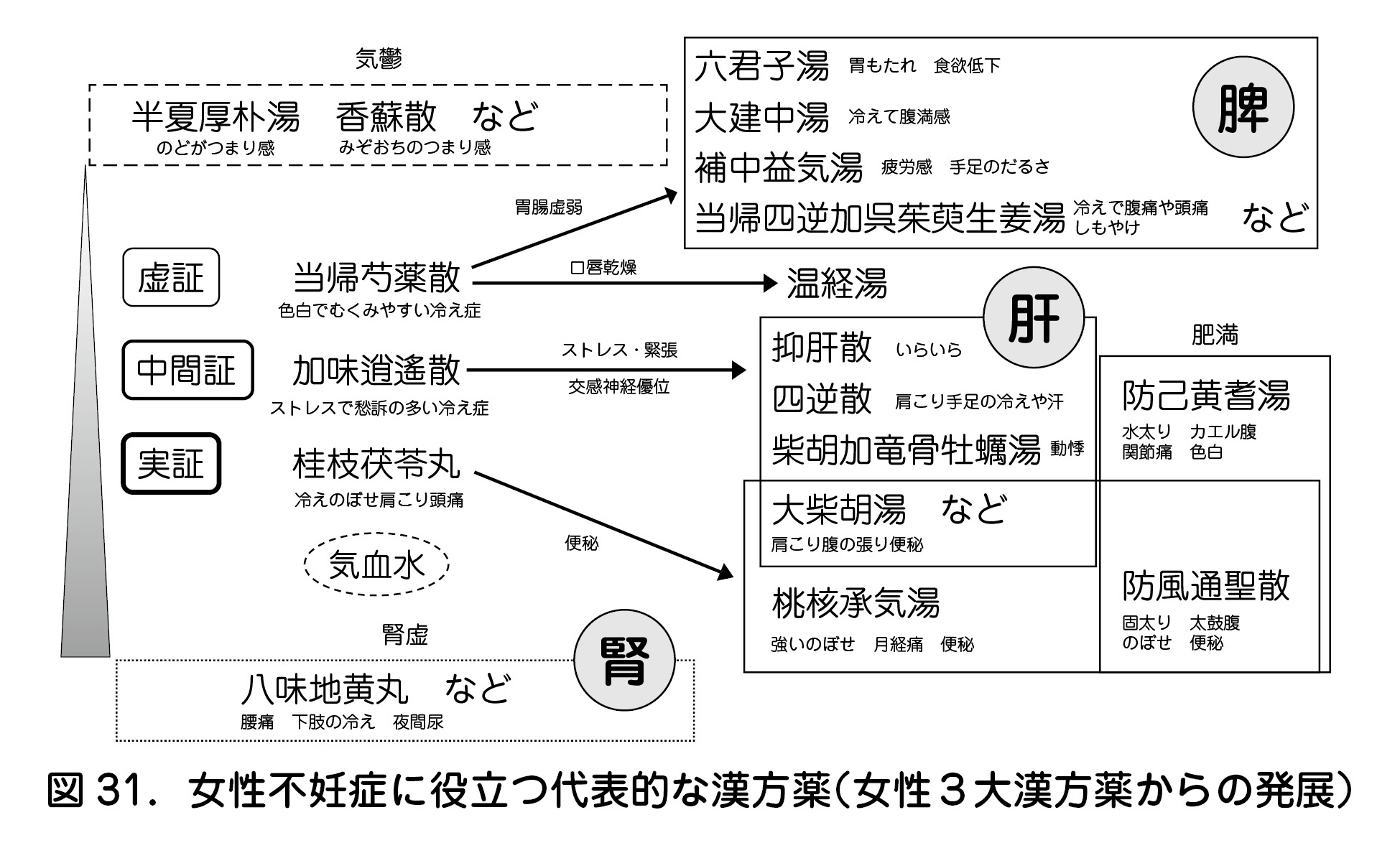
b.女性不妊症に役立つ代表的な漢方薬(女性3大漢方薬からの発展)
女性不妊症に役立つ代表的な漢方薬について図31のフローチャートにまとめた.
当帰芍薬散内服で胃腸の具合が悪くなる場合は六君子湯などの「補脾剤」,口唇乾燥や手のほてりがある場合は温経湯(うんけいとう)を考慮する.加味逍遙散でいらいらが落ち着かない場合は抑肝散(よくかんさん),緊張が強く手足に冷えや汗をかく場合は四逆散(しぎゃくさん),動悸が強い場合は柴胡剤を柴胡加竜骨牡蠣湯(さいこかりゅうこつぼれいとう)に変更する.桂枝茯苓丸で便秘がある場合は桃核承気湯(とうかくじょうきとう),高年女性や夜間尿や腰痛,足腰の冷えなどの腎虚の症状があれば八味地黄丸,気鬱の際には半夏厚朴湯(はんげこうぼくとう)や香蘇散(こうそさん)を考慮する.
c.女性不妊症に役立つ代表的な漢方薬(各論)
ア 排卵障害に対する漢方薬
イ 子宮内膜の状態を改善する漢方薬
ウ 漢方薬の作用機序(抜粋)
当帰芍薬散,温経湯はFSH,LH,エストラジオールの増加をもたらし排卵障害に有効と報告されている.温経湯は下垂体性ゴナドトロピンの律動性パターンを改善させ,卵胞成熟,排卵機構の改善とともに黄体機能を向上させることが示されており,クロミフェン無効の無排卵周期症に対する有効性やIVF-ETでの受精卵の分割が進み胚形成に促進的に働く可能性も報告されている.





