16.オンコロジーエマージェンシー(oncology emergency)
・ オンコロジーエマージェンシーとは悪性腫瘍のために緊急な対応が必要となる症状の総称であり,表26 のような事態が列挙される1).
・ これらの病態を理解・診断し,迅速に対応することが臨床腫瘍医にとって重要な資質の1 つである.

以下,オンコロジーエマージェンシーの病態別対応を述べる.
(1)代謝障害
1 )高カルシウム血症
①病態,症状,頻度
・ 悪性腫瘍による高カルシウム血症の機序としては,腫瘍から分泌される副甲状腺ホルモン関連蛋白(PTHrP:parathyroid hormone-related protein)によるhumoral hypercalcemia of malignancy(HHM,扁平上皮癌で多い)と広範な骨転移に伴うlocal osteolytic hypercalcemia に分類される.一般にHHM の方が治療抵抗性である.
・ 婦人科がんにおいては,全体では5%程度にみられるとされる2).卵巣癌では頻度が高く,特に小細胞癌,明細胞癌では高頻度とされている3).
②治療(表27)
a.細胞外液量の補充と利尿
・ 高カルシウム血症は食欲不振と利尿を来し,脱水状態とそれによる腎機能不全を伴い,これがさらに高カルシウム血症を悪化させるという悪循環に入っていることが多い.
・ したがって,輸液により細胞外液を補充し,尿へのカルシウム排泄を促進することが重要である.なお,乳酸リンゲル液,高カロリー輸液製剤の多くは大量のカルシウムを含んでいること,またサイアザイド系利尿薬はカルシウム排泄を抑制することに注意が必要である.

b.ビスホスホネート(BP)
・ 強力な破骨細胞抑制効果を持ち,また副作用が少ない.現在は最も効力の高いゾレドロン酸が使われている.ゾレドロン酸は4㎎を生理食塩水または5%ブドウ糖溶液 500mL に溶解し,15 分で点滴する.
・ 血清カルシウムは 2 日後から低下し始め,6~10 日で最低となる.副作用としては,発熱・感冒様症状を10~20%に認めるが,特に処置が必要な場合は稀である.
c.カルシトニン
・ エルシトニンⓇ 40 単位を生食50mL で点滴静注または筋注で 1 日 2 回投与する.数時間で効果があるが 2,3 日で不応性となる.
・ 急速にカルシウムを低下させる必要がある緊急時にはビスホスホネートと併用される.
d.ステロイド
・ 特に血液腫瘍による高カルシウム血症で有用で,通常プレドニゾロンⓇ20~50㎎ /dayの経口投与または点滴静注を行う.
e.デノスマブ(denosumab)
・ ビスホスホネート耐性の高カルシウム血症においての効果が報告されている.
・ 1 カ月以内のビスホスホネート投与にもかかわらずcCa > 12.5㎎ /dL の患者に対して,デノスマブ120㎎をD1,8,15,29,その後 4 週ごとに投与したところCaは投与後 4 日目前後に低下開始し,2 週後には大部分で正常化しており,有効なことが示された4).
2 )腫瘍崩壊症候群(TLS:tumor lysis syndrome)
①病態,症状,頻度
・ 腫瘍が急激に崩壊するため細胞内物質が血液中に大量に放出され,生命にかかわる危険な状態を来す.
・ 化学療法が多いが,放射線療法,ホルモン療法,分子標的療法,免疫療法でも起こり,分子標的・免疫療法では遅く発現することがある.
・ 高尿酸血症による腎不全,高カリウム血症による心不整脈,高リン血症,低カルシウム血症による筋痙攣,テタニー,心不整脈が問題になる.
・ 婦人科がんでの頻度は低いが,各腫瘍において,症例報告がある5).
②治療
・ 治療開始前にリスクの高い患者(表28)を認識し,予防することが重要である(表29).
・ 可能であれば治療開始前 24~48 時間から十分な輸液を開始し,十分な利尿をつける.尿アルカリ化により尿酸は溶けやすくなるが,ヒポキサンチン,カルシウムは析出しやすくなるため推奨されない.
・ アロプリノール,フェブキソスタット:リスクのある間はアロプリノール300~900㎎ /day あるいはフェブキソスタット600㎎を経口で投与する.比較試験での尿酸低下はアロプリノール200~600㎎ /day<フェブキソスタット120㎎ /day,アロプリノール300㎎ /day=フェブキソスタット 60㎎ /day と考えられる.
・ 治療開始後数日は毎日電解質,尿酸をチェックする.カリウム,カルシウム異常のある場合は心電図モニターを行うとともに輸液で補正する.
・ 腎不全出現時は早めに透析を行い,電解質を補正する.
・ ラスブリカーゼ: 尿酸代謝酵素,アロプリノールよりも急速かつ著明に尿酸値を低下させ,またキサンチンを増加させないので尿アルカリ化不要という利点がある.0.2㎎ /㎏ /day for 3-7 days(day 0 or day1-)を投与する.副作用として頭痛,発疹,アナフィラキシー(1%以下)が挙げられる.


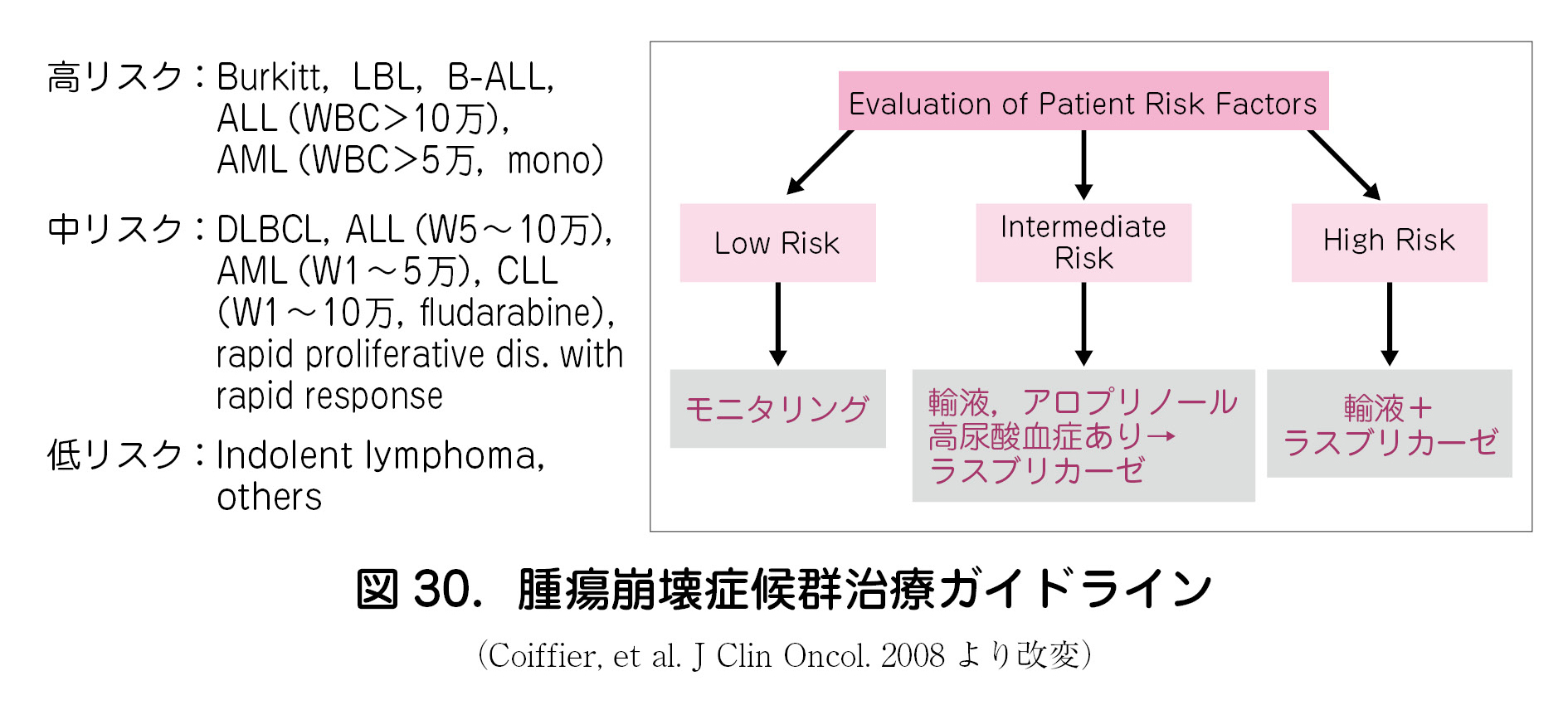
③ガイドライン(図30)
・疾患により高・中・低リスクに分ける6).
治療方針は
低リスク:モニタリング
中リスク:輸液とアロプリノール
高リスク:輸液とラスブリカーゼ
3 )低ナトリウム血症
①病態,症状
・ ほとんどの場合異常な水の貯留が主因で,過量の水分の投与が加わる場合も多い.異常な水分貯留は抗利尿ホルモン(ADH)の異常な分泌による.
・ 主に脳浮腫による精神神経症状がみられるが,重症度および進行速度による.一般的に115 mEq/L 以下になると意識障害,痙攣の危険性が高まる.
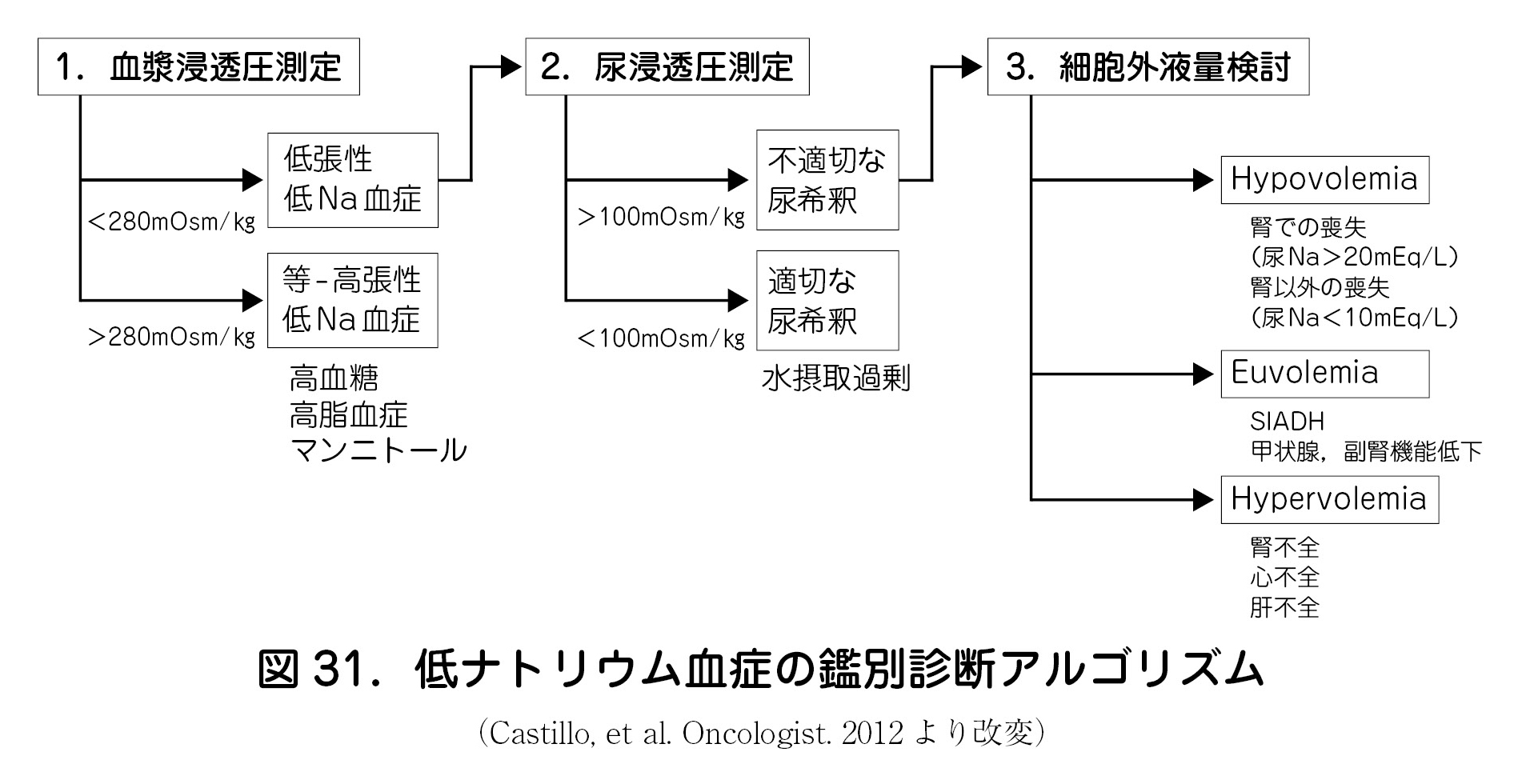
②鑑別診断
・ ADH 分泌異常の原因として,体液量増減の評価が重要である(図31)7).
a.循環血漿量低下による末梢循環の低下
・ 浮腫・胸腹水と塩分貯留を伴う低ナトリウム血症:肝機能低下,悪性胸腹水貯留,静脈閉塞,心不全などがん患者の病態に伴いしばしば見られる.
・ 脱水状態を伴う低ナトリウム血症:重症下痢,急性出血,胸腹水の排液,イレウスなどで起こる.尿からのNa 喪失はシスプラチンによる塩分喪失性腎症,副腎不全,サイアザイドの使用,あるいはくも膜下出血・頭蓋内手術に伴う中枢性の塩分喪失などで起こる.
b. 循環血漿量低下を伴わない低ナトリウム血症(抗利尿ホルモン不適切分泌症候群,SIADH)
・ 腎集合管における水再吸収が促進されるので,体液量が増加し希釈性低Na 血症が起こる.種々の腫瘍,頭蓋内疾患,肺疾患,薬剤に伴って起こる.
・ 腫瘍からのADH 分泌は肺小細胞癌が最も多いが種々の腫瘍で起こり得る.婦人科領域でも,子宮頸癌,卵巣などの小細胞癌に伴うADH 分泌が報告されている8).
・ 原因薬剤としてはビンカアルカロイド,サイクロフォスファミド,メルファランなどが多い.抗がん薬以外ではニコチン,カルバマゼピン,バルビツレート,モルヒネ,SSRI などが知られている9).
・ SIADH の診断基準:1)低ナトリウム血症,低浸透圧血症,2)尿中ナトリウム排泄20mEq/L 以上,3)尿浸透圧>血漿浸透圧,4)脱水症状なし,5)副腎,甲状腺,腎機能正常.
③治療
・表30 に示す.

(2)構造的障害
1 )頭蓋内圧亢進
①病態,症状,頻度
・ 腫瘍に伴う脳転移,脳出血,髄膜炎などによる脳圧亢進;頭痛,嘔気,意識障害,脳神経障害などが生じる.婦人科がんでは稀であるが,注意すべき症候群である10).
②治療
・ 頭蓋内圧亢進が疑われたらすぐに脳圧を低下させる治療を開始するべきである.
a.過換気
・ 最も迅速に効果が出るが数時間しか十分な効果がない.挿管,人工呼吸を開始しpCO2 を25~30㎜ Hg に保つ.
b.浸透圧利尿薬
・ グリセオールは使いやすく,高Na 血症の他には大きな副作用はない.200mL を1日2 回から開始し,最高1,000~1,500mL/day まで投与可能.
・ マンニトールは即効性が高いがリバウンドや電解質異常が起こりやすい.
c.ステロイド
・ 脳転移に伴い浮腫がある場合は特に有効である.デキサメタゾン8~12㎎ /day を1 週間程度投与し,漸減していくことが多い.
2 )脊髄圧迫
①原因疾患,症候,頻度
・ 肺癌,乳癌,前立腺癌が多く,各20%前後を占める.
・ 背部痛が初発症状として多い.他に歩行障害,感覚障害,自律神経障害などがある.
・ これも婦人科がんでは骨転移が比較的少ないこともあり,稀であるが脊髄圧迫で発見された症例の報告がある11).
②診断
・ MRI が中心で,感受性44~93%,特異性90~98%とされる.
③治療
・ 放射線療法が中心になるが,必ず手術の適応について整形外科と検討する必要がある.
a.放射線照射
・ 回復例は不全麻痺例で43%,完全麻痺例で14%と報告されている.dose/fractionについて標準方法は確立していない.
b.ステロイド
・ 浮腫による悪化を防ぎ,照射と併用必要.デキサメタゾン100㎎ vs 10㎎:回復25% vs 8%(p = 0.22),維持デキサメタゾンvs なし:回復81% vs 63%(p = 0.046)との報告がある.
c.手術
・ 適応は照射既往・照射中の悪化,圧迫骨折など.除圧術+ RT の方がRT 単独より有効との比較試験がある.
3 )上大静脈症候群
①病態,症状,頻度
・ 腫瘍の上大静脈圧迫による症候群で,頭部・頸部・上肢の浮腫・うっ血・静脈拡張,喉頭・咽頭浮腫を来す.原因は肺癌が大半を占め, 婦人科がんでは稀である.
②診断
・ 造影CT にて静脈血栓症の鑑別,腫瘍の診断を行う.
③治療
a.保存的治療
・ ステロイド(デキサメタゾン4㎎ /6hrs),フロセミドなどが使われるが,明らかなエビデンスはない.
b.放射線照射
・ 肺小細胞癌の78%,非小細胞癌の63%で症状改善が見られる.
c.化学療法
・ 非ホジキンリンパ腫・肺小細胞癌の80%,肺非小細胞癌の40%で症状消失する.
d.ステント留置
・ 75~100%で48~72 時間以内に改善,再発率15%,合併症(感染,肺塞栓,出血,穿孔)
3~7%と報告されている.
4 )心囊水貯留(心タンポナーデ)12)
①病態,病因,頻度
・ 剖検においてはがん患者の10~15%で心囊水が認められる.大部分は肺癌,乳癌の転移によるが,他はリンパ腫,白血病,胸壁照射,化学療法などに伴う.婦人科がんでは稀であるが,種々のがん種で報告されている13, 14).
②診断
・ 呼吸困難,起坐呼吸,動悸,疲労,めまい;頻脈,気脈,頸部静脈怒張,脈圧低下など.心エコー,CT でほぼ診断可能.
③治療
・ タンポナーデ症状がある場合は心囊穿刺,心膜開窓を行う.30 日間のコントロール率は穿刺のみでは50%とされており,心囊内注入によるコントロール率はテトラサイクリン80~90%,ブレオマイシン75%,チオテパ0% , シスプラチン90%,OK- 432(ピシバニールⓇ)70%と報告されている.最近Bevacizumab の有効性も報告されている.
(3)治療に伴うオンコロジーエマージェンシー
1 )血管新生阻害薬に伴う出血15,16)
・ 種々の血管新生阻害薬の有効性が明らかになり卵巣癌,子宮癌でも用いられているが,その副作用の1 つとして出血が挙げられる.
・ 機序としては内皮細胞再生能力低下・アポトーシス誘導→血管脆弱化,細胞外基質の減少,血小板機能低下などが挙げられている.
・ リスク因子としては扁平上皮がん,血痰,食道静脈瘤などが挙げられている.
2 )免疫関連有害事象
・ PD- 1,PD-L1 などを阻害する免疫チェックポイント治療の有効性が明らかになっている.
・ 頻度は低いが劇症Ⅰ型糖尿病,副腎不全,心筋炎,脳炎(表31)などオンコロジーエマージェンシーとして対応が必要な有害事象が生じている.

・ 臨床腫瘍学会がん免疫療法ガイドライン17),ASCO ガイドライン18),各製薬会社の適正使用ガイドなどを参考にして,各施設での治療方針を決定する必要がある.
・ がん研ではTEAM IT(immunotherapy)として多診療科,多職種で検討してマニュアルを作成し,対応,治療方針を検討している(表32).

文献
1)Marinella MA. Handbook of Cancer Emergencies. Jones & Bartlett Pub. 2009.
2) Lim D, Oliva E. Gynecological neoplasms associated with paraneoplastic hypercalcemia. Semin Diagn Pathol.
2019, 36, 246-259.
3) Callegaro-Filho D, Gershenson DM, Nick AM, et al. Small cell carcinoma of the ovary-hypercalcemic type
(SCCOHT): A review of 47 cases. Gynecol Oncol. 2016, 140, 53-57.
4) Hu MI, Glezerman I, Leboulleux S, et al. Denosumab for patients with persistent or relapsed hypercalcemia
of malignancy despite recent bisphosphonate treatment. J Natl Cancer Inst. 2013, 105, 1417-1420.
5) Ito T, Ohta T, Narumi M, et al. Tumor lysis syndrome associated with docetaxel and carboplatin in a case
with recurrent endometrial cancer. Gynecol Oncol Rep. 2018, 24, 21-23.
6) Coiffier B, Altman A, Pui CH, et al. Guidelines for the management of pediatric and adult tumor lysis
syndrome: an evidence-based review. J Clin Oncol. 2008, 26, 2767-2778.
7) Castillo JJ, Vincent M, Justice E. Diagnosis and management of hyponatremia in cancer patients. Oncologist.
2012, 17, 756-765.
8) Kim DY, Yun HJ, Lee YS, et al. Small cell neuroendocrine carcinoma of the uterine cervix presenting with
syndrome of inappropriate antidiuretic hormone secretion. Obstet Gynecol Sci. 2013, 56, 420-425.
9) Ellison DH, Berl T. Clinical practice. The syndrome of inappropriate antidiuresis. N Engl J Med. 2007, 356,
2064-2072.
10) Zhang Y, Grant MS, Stepp WH, et al. Clinical characteristics of CNS metastases from primary gynecologic
cancers. Gynecol Oncol Rep. 2019, 30, 100518.
11) Liu A, Sankey EW, Goodwin CR, et al. Postoperative survival and functional outcomes for patients with
metastatic gynecological cancer to the spine: case series and review of the literature. J Neurosurg Spine.
2016, 24, 131-144.
12) Maisch B, Seferovic PM, Ristic AD, et al. Guidelines on the diagnosis and management of pericardial
diseases executive summary; The Task force on the diagnosis and management of pericardial diseases of the European society of cardiology. Eur Heart J. 2004, 25, 587-610.
13) Liu G, Zhang Q, Li Z, et al. Endometrial carcinoma complicated by malignant pericardial effusion: A case
report on the therapeutic regimen. Medicine( Baltimore). 2019, 98, e17584.
14) English E, McNally L, Chen MD. Fatal cardiac tamponade following cytoreductive surgery for serous
carcinoma of the ovary. Gynecol Oncol Rep. 2015, 13, 76-78.
15) Keefe D, Bowen J, Gibson R, et al. Noncardiac vascular toxicities of vascular endothelial growth factor
inhibitors in advanced cancer: a review. Oncologist. 2011, 16, 432-444.
16) Wu YS, Shui L, Shen D, et al. Bevacizumab combined with chemotherapy for ovarian cancer: an updated
systematic review and meta-analysis of randomized controlled trials. Oncotarget. 2017, 8, 10703-10713.
17)公益財団法人臨床腫瘍学会.がん免疫療法ガイドライン 第2 版.金原出版.2019.
18) Brahmer JR, Lacchetti C, Schneider BJ, et al. Management of Immune-Related Adverse Events in Patients
Treated With Immune Checkpoint Inhibitor Therapy: American Society of Clinical Oncology Clinical
Practice Guideline. J Clin Oncol. 2018, 36, 1714-1768.





